El Dr. Gregory Riggins, catedrático de Neurocirugía y Oncología de la Universidad Johns Hopkins, y su grupo de investigación suelen encontrar pocas o ninguna dificultad a la hora de permitir el crecimiento del cáncer en ratones de prueba para sus estudios.
Sin embargo, durante un periodo de varios meses en 2009, hubo un grupo de estos ratones en los que el desarrollo tumoral simplemente no se produjo. Tras un examen más detallado, descubrieron que este resultado inesperado se debía a que a estos roedores se les había administrado fenbendazol como tratamiento antiparasitario.
«En nuestra exploración de varios medicamentos dentro de este grupo en particular, el fenbendazol surgió como el más eficaz. Esto llamó nuestra atención». Dijo el investigador
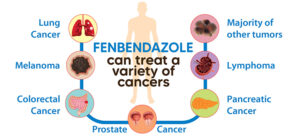
Cuando empezaron a difundirse noticias sobre sus capacidades, las personas descubrieron que el fenbendazol podía administrarse solo o combinado con otros procedimientos para curar o dificultar el crecimiento del cáncer.
Riggins y Gallia, junto con su equipo de investigación, iniciaron un plan no sólo para comprender cómo funciona este medicamento, sino también para mejorar su utilidad contra las células del glioblastoma y conseguir producirlo para ensayos con pacientes. Según el sistema de creencias de estos investigadores, el fenbendazol ayuda a bloquear el desarrollo tumoral frenando la formación de filamentos de tubulina, proteínas vitales para la proliferación de células cancerosas.
Este hecho ocurrió hace más de una década. En la actualidad, con el paso del tiempo, hemos adquirido conocimientos sustanciales sobre el empleo eficaz del fenbendazol para aumentar nuestras probabilidades de erradicar el cáncer.
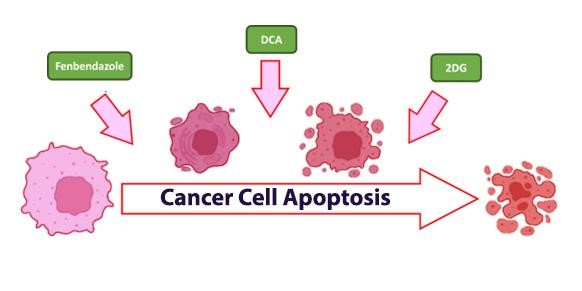
Los medicamentos renovados están logrando avances notables en el tratamiento del cáncer. Al comprender cómo utilizan la energía las células cancerosas, vemos cómo compuestos como el fenbendazol, el DCA (dicloroacetato de sodio) y el 2DG (2-deoxi-D-glucosa) revolucionan tratamientos estándar como la quimio y la radiación, ofreciendo nuevas esperanzas en el cuidado del cáncer.
La estructura energética del cáncer
En 1923, Otto Heinrich Warburg, un importante bioquímico alemán, médico en ejercicio y Premio Nobel, hizo un descubrimiento de valor incalculable que desempeñó un papel fundamental en la comprensión del patrón del metabolismo energético de las células cancerosas. Este fenómeno observado en particular se reconoce actualmente como la característica clave del cáncer apodado más comúnmente como «El Efecto Warburg».
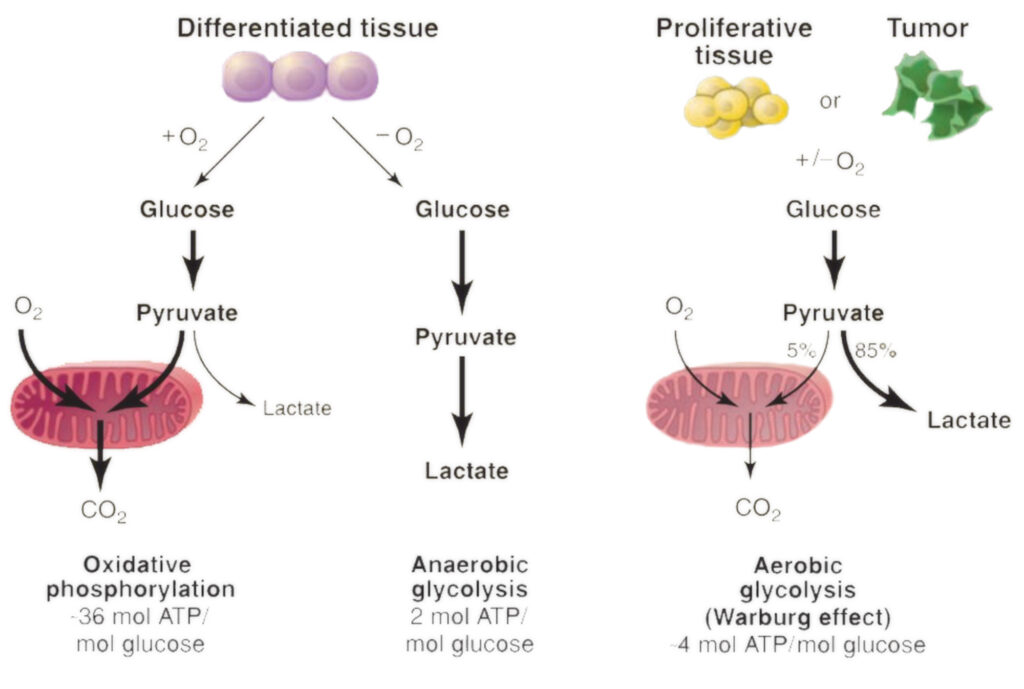
El Sr. Warburg hizo una observación notable al estudiar células tumorales de ratas: observó que prosperaban con niveles excepcionalmente altos de glucosa (azúcar), en lugar de aumentar el uso de oxígeno para el crecimiento, lo que parecía contrario a la intuición, ya que la extracción de energía de los nutrientes a través de mayores tasas de utilización de oxígeno habría sido un proceso muy eficiente.
La constatación de tales hallazgos en aquellos tiempos, hace unos cien años, despertó una gran curiosidad que dio lugar a preguntas sin respuesta más que a soluciones disponibles.
La gran avidez de glucosa y la disminución del consumo de oxígeno confieren a las células cancerosas un conjunto distinto de beneficios evolutivos. Una de las formas en que el efecto Warburg ayuda a las células malignas es facilitando la rápida acumulación de biomasa. El aumento de la captación de glucosa proporciona al tejido tumoral un exceso de componentes básicos para crear nuevo material genético y proteínas, lo que conduce a un aumento tanto de la proliferación como de la expansión del cáncer.
Además, no es ningún secreto que las células normales de los mamíferos necesitan un flujo constante de oxígeno o, de lo contrario, perecen rápidamente. Sin embargo, sus homólogas enfermas se comportan de forma totalmente diferente: el rápido crecimiento de los tumores a menudo supera su suministro de O2 disponible, pero no se ralentiza debido a su naturaleza adaptativa, sino que prospera en tales circunstancias sin asfixiarse.
En poco tiempo, las células cancerosas cambian su proceso metabólico a la glucólisis dependiente del oxígeno. Comienzan a generar y verter abundantes cantidades de ácido láctico más allá de los límites celulares, lo que provoca un aumento de las condiciones ácidas en el entorno del tumor.
El aumento de la acidez de tales entornos cancerosos refuerza aún más la penetración y la propagación mediante la degradación de la matriz extracelular de conexión celular de nuestro cuerpo. Cuando este nivel de acidez aumenta, ayuda a los tumores malignos a eludir nuestro mecanismo de inmunidad, una protección inherente contra este tipo de enfermedades. Es innegable que esta es una de las razones por las que la inmunoterapia tiende a perder su efecto en las fases avanzadas del cáncer.
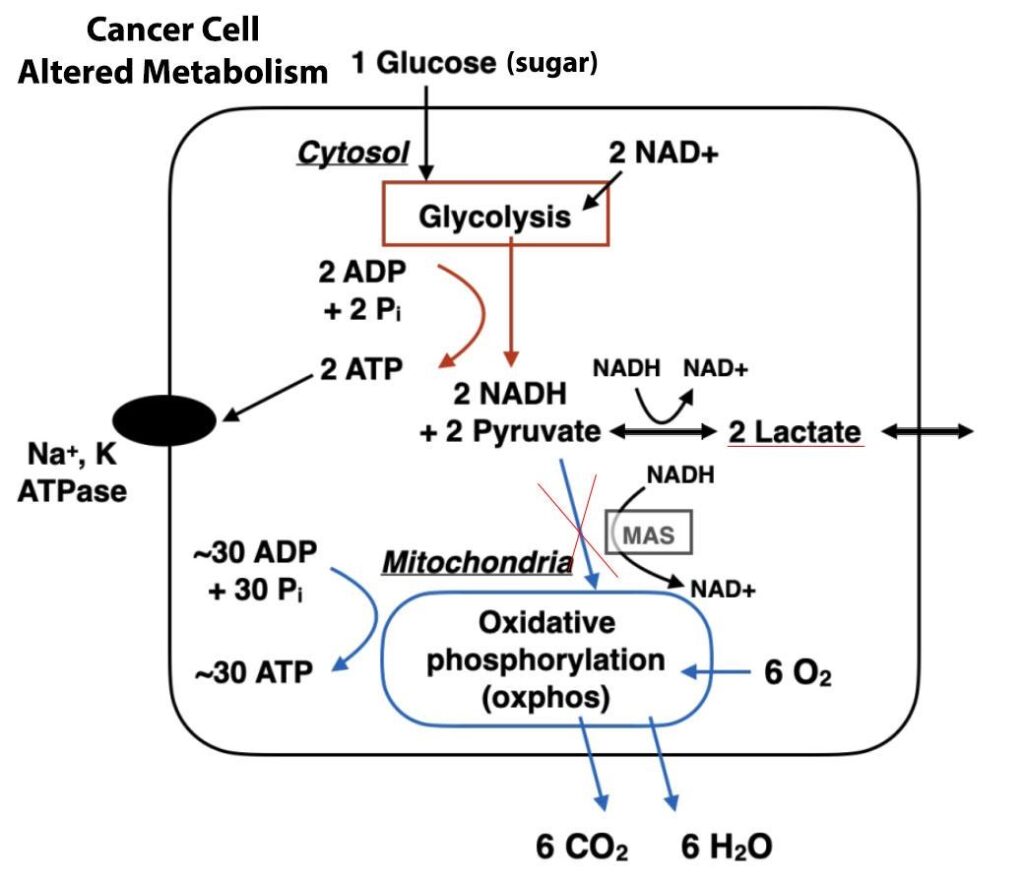
Al mismo tiempo, las células cancerosas consumen menos oxígeno, por lo que las mitocondrias generan menos especies reactivas del oxígeno. Estas especies son cruciales para detener y eliminar las células cancerosas dañinas. La enfermedad empieza a esquivar un mecanismo denominado apoptosis.
La apoptosis es un fenómeno ordinario que entra en juego en nuestro cuerpo; elimina convenientemente las células no deseadas o excesivas de continuar su existencia con la anatomía.
Se trata esencialmente de una muerte celular natural preestablecida que detiene el crecimiento tumoral en su inicio exterminándose a sí misma principalmente para prevenir cualquier posible expansión innecesaria de estos tumores dentro de nosotros causando daños irreparables, haciendo así que los cuerpos celulares malignos sean incesantes.
Se trata de ventajas metabólicas clave que permiten la progresión no regulada del ciclo vital de diversas transformaciones mientras prosperan indefinidamente siendo inmortales debido a la disuasión de las muertes programadas oportunas (Apoptosis).
Mención aparte merece el enrevesado proceso evolutivo que experimentan las metamorfosis neoplásicas, que tienden a desafiar a los médicos, convirtiéndolas en adversarios formidables que exigen complejos protocolos de tratamiento, sin olvidar otro aspecto: el aprovechamiento del efecto Warburg contra las sustancias carcinógenas.
En términos de identificación de enfermedades, la humanidad ha utilizado este fenómeno del metabolismo del cáncer con fines de detección. La prueba conocida como tomografía por emisión de positrones (PET) pone de relieve los tejidos y órganos con una actividad metabólica inusual.
Como las células cancerosas presentan el efecto Warburg, absorben glucosa radiactiva a una velocidad cientos de veces superior a la del tejido normal que las rodea. En consecuencia, los tumores se iluminan en las imágenes resultantes, lo que facilita su seguimiento por todo el cuerpo.
En lo que respecta al tratamiento, el hecho de que casi todos los tratamientos anticancerígenos anteriores se hayan centrado exclusivamente en técnicas genéticas podría hacer que el cambio de paradigma «Warburg» se considerase un «talón de Aquiles» olvidado en cualquier enfoque dirigido al tratamiento del cáncer a lo largo de casi un siglo. Un compuesto alternativo, el dicloroacetato de sodio (DCA), actúa de forma única restableciendo el equilibrio de las funciones celulares anómalas relacionadas con el metabolismo.
Necesidad de inmunoterapia
Las células cancerosas han desarrollado diversos mecanismos para camuflarse, lo que las hace indetectables para las defensas inmunitarias de nuestro organismo. Pueden poseer mutaciones genéticas o presentar proteínas de superficie distintas; ambos factores pueden impedir que el sistema inmunitario distinga y combata estas células.
Aquí es donde las TIL son una parte integral en este escenario. Si los tumores de un paciente no contienen estas células TIL, significa que la respuesta inmunitaria defensiva no está luchando eficazmente contra el tumor maligno, por lo que es necesaria una intervención inmunoterapéutica.
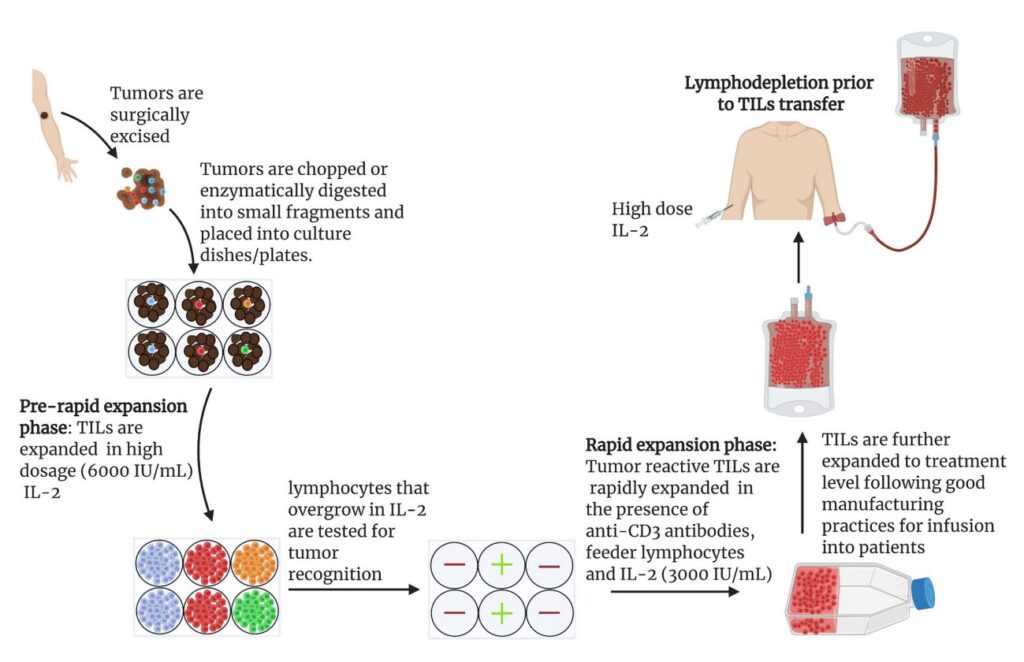
Dificultades de la inmunoterapia contra el cáncer
El tratamiento del cáncer ha entrado en una nueva fase con la inmunoterapia, lo que aporta optimismo a muchas personas. Sin embargo, este enfoque no está exento de complicaciones. Una de las principales preocupaciones es la capacidad de las células cancerosas para crear tolerancia con el paso del tiempo. Debido a su elevada producción de energía mediante el proceso de glucólisis, estas células dañinas suelen bloquear vías específicas importantes para gestionar eficazmente las funciones de las células T.
Si estas células T no maduran con precisión, no consiguen identificar y neutralizar con éxito las células tumorales de forma eficaz, por lo que se ven favorecidas por la fuerza previa obtenida de los anticuerpos terapéuticos administrados anteriormente.
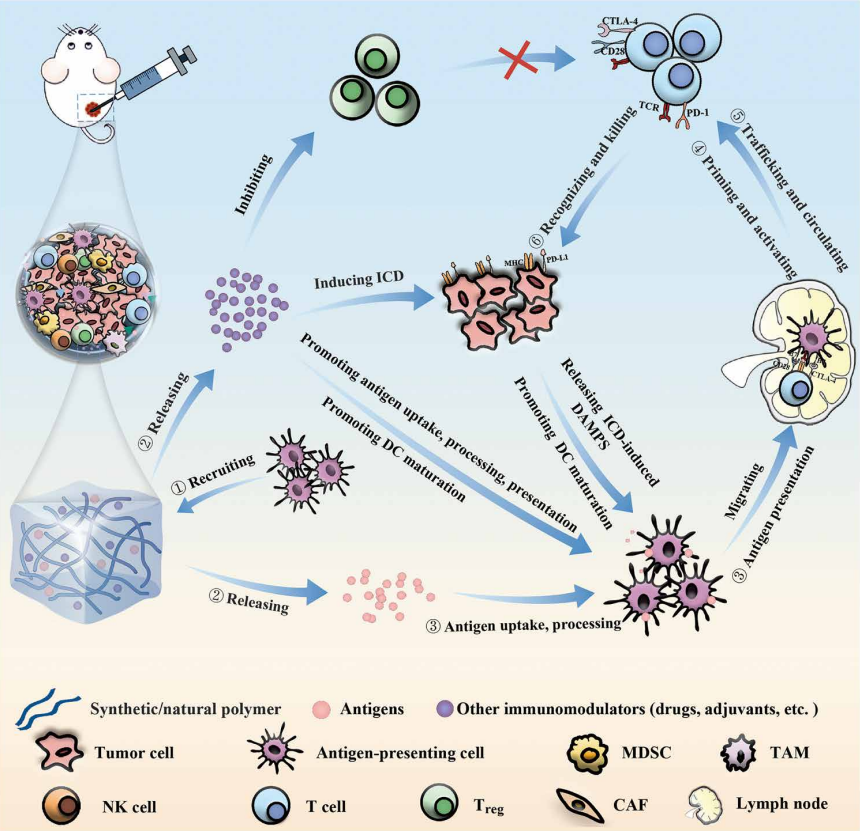
Afrontar las dificultades
En respuesta a estos obstáculos, dirigir los esfuerzos hacia la inhibición del sistema de producción de energía de las células tumorales posinmunoterapia podría resultar ventajoso. Al restringir su suministro de energía, existe la posibilidad de que sean incapaces de bloquear las vías de señalización que dictan el desarrollo y el control de las células T.
Últimos hallazgos en estudios científicos: 2-deoxi-D-glucosa (2DG)
En el tratamiento del cáncer, especialmente del cáncer de mama triple negativo (CMTN), hay un avance apasionante.
Los científicos han descubierto que la combinación de inmunoterapia con un antimetabolito de la glucosa conocido como 2DG podría aumentar la eficacia del tratamiento. Esto es especialmente destacable porque las células del TNBC suelen mostrar altos niveles de una proteína llamada ligando de muerte programada 1 (PD-L1).
El problema del tratamiento del TNBC es que sólo un pequeño grupo de pacientes, entre el 10 y el 20%, obtiene resultados positivos con las terapias dirigidas a PD-L1 o PD-1, que son agentes clave de la respuesta inmunitaria del organismo.
Este nuevo enfoque, basado en la 2DG, podría cambiar las reglas del juego para muchas pacientes con CMTN que actualmente tienen respuestas limitadas al tratamiento.
Aquí hay un punto clave: una forma particular de PD-L1, conocida como PD-L1 glicosilada, es crucial para las interacciones que tienen lugar dentro del marco PD-L1-PD-1. Es más, las células asociadas con el TNBC tienden a tener niveles más altos de este PD-L1 glicosilado en comparación con las células no TNBC.
Las investigaciones han demostrado que se puede reducir la cantidad de glicosilación en PD-L1 si se afecta significativamente a la estabilidad y la función de esta molécula procancerosa que inhibe el sistema inmunitario.
Aquí es donde entra en juego la «desoxiglucosa». El uso de la desoxiglucosa podría alterar este proceso y dar lugar a nuevas estrategias que combinen distintos enfoques para lograr resultados más eficaces en el tratamiento del TNBC.
Técnicas de tratamiento del cáncer: Métodos convencionales y progresivos
El camino hacia soluciones eficaces contra el cáncer pasa por numerosos métodos, desde las técnicas convencionales hasta las más vanguardistas.
Los procedimientos de tratamiento establecidos, como la quimioterapia y la radioterapia, gozan de un amplio reconocimiento, mientras que elementos novedosos como la 2DG se han vuelto progresivamente atractivos debido a sus posibles ventajas en el tratamiento del cáncer, ya sea individualmente o complementados con ayudas bien establecidas como el fenbendazol y el DCA, que también contribuyen significativamente a combatir la enfermedad.

Quimioterapia
La utilización de la quimioterapia sigue siendo un elemento fundamental en la lucha contra la enfermedad conocida como cáncer. Es especialmente eficaz en enfermedades como el cáncer de mama, donde se utiliza para minimizar el tamaño del tumor y facilitar su extirpación quirúrgica, un método conocido como quimioterapia preoperatoria o PCT.
Sin embargo, aunque pueda disminuir las dimensiones del tumor, no siempre podemos confiar únicamente en este método, porque hay numerosos casos en los que las células malignas reaparecen después del tratamiento.
Potenciar el efecto de la quimioterapia mediante 2DG
Los estudios indican que entrelazar la quimioterapia con la 2DG puede reforzar su eficacia. Funcionalmente similar a la glucosa, la 2DG es capaz de interferir en las actividades metabólicas de las células cancerosas, lo que podría aumentar el efecto de los tratamientos de quimioterapia habituales.
La doble utilización simboliza la posibilidad de una respuesta patológica completa, lo que implica que se pueden conseguir resultados más potentes y prolongados del tratamiento. Se han realizado numerosas pruebas de laboratorio y estudios con animales para confirmar esta estrategia combinada.
Radioterapia
Dentro de las células cancerosas, el método independiente para regular el metabolismo del azúcar es la 2DG, pero también se fusiona con formas de terapia como la quimioterapia y la radioterapia.
Siendo realistas, la radioterapia desempeña un papel crucial en el tratamiento del cáncer. Aproximadamente el 60% de las personas que luchan contra esta cruel enfermedad experimentarán este tipo de tratamiento, ya sea de forma individual o junto con otros tratamientos.
La radioterapia, aunque es una herramienta poderosa en la lucha contra el cáncer, no está exenta de dificultades. Es eficaz, sin duda, pero puede tener algunos efectos secundarios no deseados con el tiempo. Una de las principales preocupaciones es que las células cancerosas desarrollen una resistencia a la radiación, y también existe el riesgo de dañar las células sanas.
Para hacer frente a estos problemas, especialmente el de la tolerancia a la radiación, es fundamental utilizar inhibidores glucolíticos. Estos inhibidores cortan el suministro de energía a las células cancerosas, privándolas de los nutrientes que necesitan.
De este modo, a las células cancerosas les resulta más difícil repararse después de haber sido alcanzadas por la radiación, lo que conduce a su descomposición y destrucción. Se trata de un paso adelante para que la radioterapia sea más segura y eficaz para los pacientes.
Potenciación de la radioterapia mediante 2-Deoxi-D-glucosa
La 2DG es un inhibidor glucolítico. Su función consiste en unirse a la proteína transportadora de glucosa GLUT1 antes de ser fosforilada por la enzima Hexokinasa. Sin embargo, su progresión metabólica termina ahí, asegurando que la ruta glucolítica permanezca obstruida.
De este modo, las células cancerosas expuestas a este inhibidor no pueden producir energía debido a la interrupción del proceso normal de glucólisis de la glucosa. Además, el 2DG estimula las funciones de las enzimas caspasa 3 y PARP, lo que conduce a la apoptosis de las células malignas, sin afectar a las células sanas.
En el tratamiento del cáncer, se vislumbra una combinación prometedora: la 2-deoxi-D-glucosa (2DG) combinada con radioterapia. Este dúo podría aumentar considerablemente la potencia de la radioterapia. ¿Cómo?
Pues bien, la 2DG actúa como un inhibidor de la glucosa. Interfiere en la capacidad de las células cancerosas para repararse a sí mismas después de haber sido dañadas por la radiación, principalmente porque estas células están hambrientas de glucosa y nutrientes esenciales.
Pero la 2DG no es sólo un truco. Tiene múltiples funciones. Además de ser un disruptor, también amplifica el impacto de la radioterapia. Su acción está ligada a la alteración del equilibrio de los procesos de oxidación-reducción dentro de las células.
Un aspecto importante a tener en cuenta es que se cree que el estrés oxidativo es una vía clave a través de la cual la radiación ionizante mata las células cancerosas. Este nuevo enfoque, que utiliza 2DG junto con la radioterapia, podría cambiar las reglas del juego en el tratamiento eficaz del cáncer.
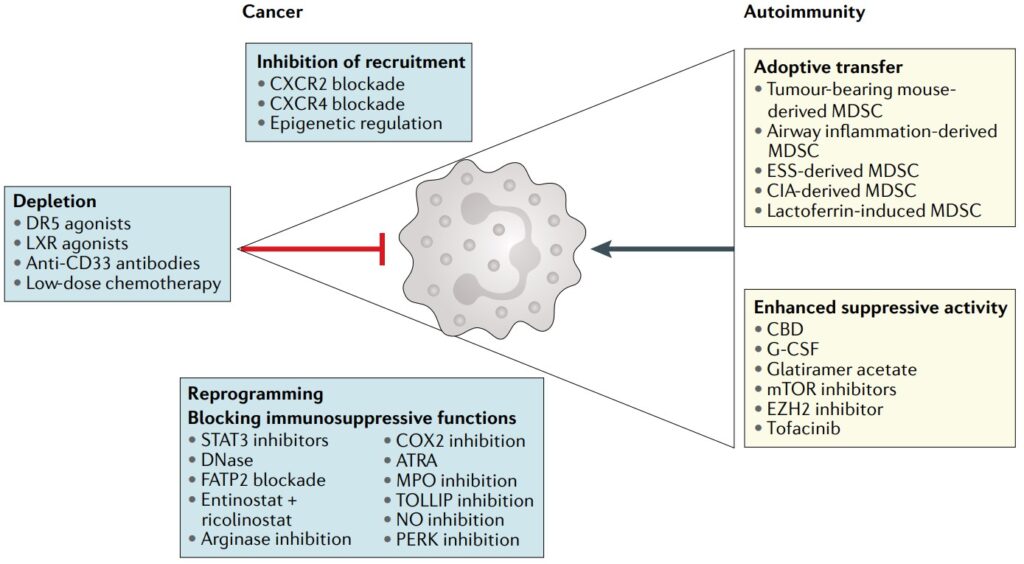
Diversidad de las células cancerosas
Las células cancerosas son un grupo diverso, algo que los científicos llaman heterogeneidad tumoral, y es algo que encontrará en casi todos los tipos de cáncer que existen. Esta diversidad suele deberse a errores cometidos durante el proceso de replicación del ADN cuando las células se dividen.
Esto es lo que ocurre: Cuando las células se dividen, si hay errores en la copia de su ADN, nacen nuevas células con mutaciones. Con el paso del tiempo, y sobre todo con determinados factores ambientales que actúan como desencadenantes, estas células mutadas pueden evolucionar y desembocar potencialmente en un cáncer. Es un proceso lento, pero así es como muchos cánceres comienzan su andadura.
Diferentes formas de disparidad en el cáncer
La diferenciación observada en las células cancerosas, denominada heterogeneidad tumoral, puede dividirse de forma sencilla en dos divisiones:
Heterogeneidad tumoral espacial.
Esto significa que las células cancerosas no se extienden uniformemente por el tejido afectado. En su lugar, tienden a extenderse de forma azarosa e impredecible.
Fluctuaciones temporales en la diversidad tumoral
A medida que los tumores se desarrollan con el tiempo, a menudo evolucionan hacia diferentes subtipos. Este proceso se conoce como heterogeneidad temporal. Esencialmente, cuanto más tiempo crece un tumor, más variado puede llegar a ser.
Las diversas características de las células tumorales plantean importantes obstáculos a la hora de combatir eficazmente el cáncer. La naturaleza diversa de estas células malignas suele provocar resistencia a las estrategias terapéuticas actuales.
Dada esta complejidad en el comportamiento del cáncer, existe una necesidad acuciante de desarrollar tratamientos que puedan dirigirse eficazmente y superar la resistencia causada por la variada composición genética que se encuentra dentro de las células cancerosas individuales.
Resultados de los ensayos
Una amplia gama de estudios, incluyendo pruebas de laboratorio, estudios en animales y ensayos clínicos en humanos, han profundizado en los efectos de la 2-deoxi-D-glucosa (2DG) en las células. Lo que se desprende de esta investigación es que la 2DG actúa de forma compleja.
No sólo detiene el proceso de glucólisis celular, sino que también favorece la apoptosis, o muerte celular programada, sin dañar las células sanas. Además, la 2DG influye en el comportamiento de los genes dentro de las células.
Altera los factores de transcripción que son clave para activar genes esenciales para la replicación celular. Esta idea apunta al potencial del 2DG como arma contra diversas características de las células cancerosas.
Una de las características de las células cancerosas son sus diversas mutaciones genéticas, que intervienen en la progresión de la enfermedad. Sin embargo, todas tienden a tener algo en común: una mayor tasa de metabolismo del azúcar en comparación con las células normales.
Esto convierte al 2DG en un tratamiento potencialmente eficaz para diversos tipos de cáncer. Funciona privando a las células cancerosas de azúcar y oxígeno, al tiempo que afecta a su actividad genética. Este enfoque puede ralentizar el crecimiento celular y dirigirlas hacia la autodestrucción, evitando un crecimiento excesivo.
Cura prospectiva del cáncer de glioblastoma
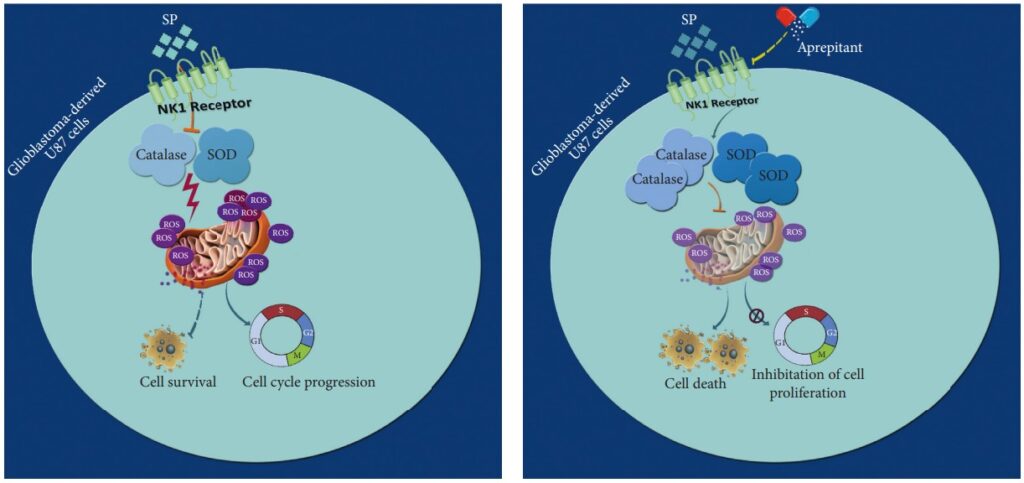
El glioblastoma destaca como una forma especialmente agresiva de cáncer cerebral, conocida por su fuerte resistencia a la muerte celular y el escaso éxito de los tratamientos actuales. Esta situación subraya la urgente necesidad de explorar nuevas opciones de tratamiento.
No hace mucho, el Dr. Evangelos Michelakis, un dedicado científico médico, y su equipo se embarcaron en varios proyectos de investigación centrados en la terapia del glioblastoma multiforme (GBM). Se dieron cuenta de que un tratamiento ideal debería ser capaz de atravesar la barrera hematoencefálica y dirigirse específicamente a las células cancerosas, sin dañar los tejidos sanos.
Su elección, el dicloroacetato sódico (DCA), reunía estas cualidades y, lo que es más importante, no mostraba signos de causar daños en la sangre, el corazón, los riñones o el hígado.
Este descubrimiento les llevó a realizar un estudio histórico con pacientes reales, que allanó el camino para otros descubrimientos revolucionarios en el tratamiento del GBM.
Impacto del DCA en la muerte de las células cancerosas y el desarrollo tumoral
Cada vez está más claro que el dicloroacetato (DCA) tiene un impacto significativo en la lucha contra el cáncer, especialmente en el caso del glioblastoma, una forma mortal de cáncer cerebral. El DCA tiene la capacidad de inducir la muerte de las células cancerosas, reducir los vasos sanguíneos que alimentan los tumores y ralentizar el crecimiento de este agresivo cáncer.
Lo que resulta especialmente prometedor es que el DCA podría ser más eficaz cuando se utiliza junto con otros tratamientos, ofreciendo un nuevo rayo de esperanza en la lucha contra esta difícil enfermedad.
Junto a otras terapias para el glioblastoma
En una oportunidad poco frecuente, los científicos tuvieron la oportunidad de comparar el tejido cerebral de pacientes antes y después de ser tratados con DCA. Lo que observaron fue alentador: una reducción de las células cancerosas en el tejido cerebral tras el tratamiento.
Esto se atribuyó a un aumento de la destrucción de células mortales y a una disminución del crecimiento de células malignas de glioblastoma multiforme. La investigación concluyó que la combinación del DCA con otros tratamientos podría ser una estrategia eficaz contra el GBM.
El equipo de investigadores sugiere utilizar el dicloroacetato, conocido por no ser tóxico, antes o después de procedimientos como la radioterapia o la cirugía. Este enfoque podría potenciar los beneficios de los tratamientos estándar para el GBM.