Dr. Gregory Riggins, professor neurochirurgie en oncologie aan Johns Hopkins, ondervindt samen met zijn onderzoeksgroep doorgaans weinig tot geen problemen bij het laten groeien van kanker in testmuizen voor hun onderzoek.
Maar gedurende een aantal maanden in 2009 was er een groep muizen waarbij de tumor zich gewoon niet ontwikkelde. Bij nader onderzoek ontdekten ze dat dit onverwachte resultaat te wijten was aan het feit dat deze knaagdieren fenbendazol toegediend hadden gekregen als een antiparasitaire behandeling.
“In ons onderzoek naar verschillende medicijnen binnen deze specifieke groep, kwam fenbendazol naar voren als het meest effectief. Dit trok onze aandacht.” Zei de onderzoeker
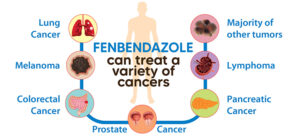
Toen het nieuws zich begon te verspreiden over de mogelijkheden, ontdekten mensen dat fenbendazol alleen of in combinatie met andere procedures kon worden toegediend om kanker te genezen of de groei ervan te belemmeren.
Riggins en Gallia begonnen samen met hun onderzoeksteam een plan om niet alleen te begrijpen hoe dit medicijn werkt, maar ook om het nut ervan tegen glioblastoomcellen te vergroten en het te produceren voor proeven met patiënten. Volgens het geloofsysteem van deze onderzoekers helpt fenbendazol bij het blokkeren van de ontwikkeling van tumoren door de vorming van tubulinestrengen tegen te gaan – eiwitten die van vitaal belang zijn voor de proliferatie van kankercellen.
Deze gebeurtenis vond meer dan tien jaar geleden plaats. Na verloop van tijd hebben we veel kennis opgedaan over het effectief gebruik van fenbendazol om onze kans op het uitroeien van kanker te vergroten.
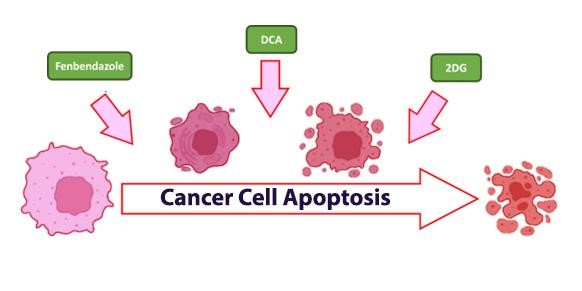
Vernieuwde medicijnen maken opmerkelijke vooruitgang in de behandeling van kanker. Door te begrijpen hoe kankercellen energie gebruiken, zien we hoe verbindingen als fenbendazol, DCA (natriumdichlooracetaat) en 2DG (2-deoxy-D-glucose) een revolutie teweegbrengen in standaardbehandelingen als chemo en bestraling en nieuwe hoop bieden in de kankerzorg.
De energiestructuur van kanker
In 1923 onthulde Otto Heinrich Warburg – een belangrijke Duitse biochemicus, praktiserend arts en Nobelprijswinnaar – een ontdekking van onschatbare waarde die een belangrijke rol speelde bij het begrijpen van het energiestofwisselingspatroon van kankercellen. Dit specifieke waargenomen fenomeen wordt tegenwoordig erkend als het belangrijkste kenmerk van kanker, beter bekend als “Het Warburg Effect”.
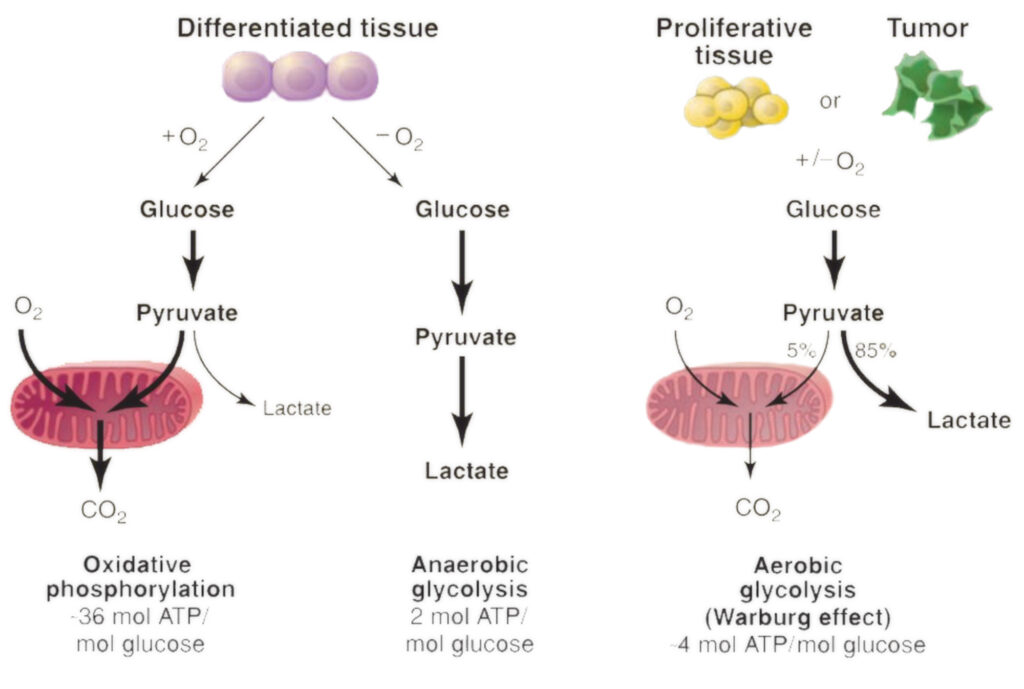
Een opmerkelijke observatie van de heer Warburg was tijdens het bestuderen van rattentumorcellen: hij merkte op dat deze bloeiden op uitzonderlijk hoge niveaus van glucose (suiker) in plaats van het gebruik van zuurstof te verhogen voor groeidoeleinden, wat tegenintuïtief leek gezien het extraheren van energie uit voedingsstoffen via een hoger gebruik van zuurstof een grotendeels efficiënt proces zou zijn geweest.
De vaststelling van dergelijke bevindingen in die tijd, zo’n honderd jaar geleden, wekte een aanzienlijke nieuwsgierigheid op die leidde tot onbeantwoorde vragen in plaats van beschikbare oplossingen.
Het enorme verlangen naar glucose en het verminderde zuurstofverbruik geven kankercellen een aantal evolutionaire voordelen. Eén manier waarop het Warburg-effect kwaadaardige cellen helpt, is door een snelle ophoping van biomassa mogelijk te maken. De verhoogde opname van glucose voorziet het tumorweefsel van overtollige bouwstenen om nieuw genetisch materiaal en eiwit aan te maken, wat leidt tot een toename in de proliferatie en uitbreiding van kanker.
Bovendien is het geen geheim dat normale zoogdiercellen een constante zuurstofstroom nodig hebben, anders gaan ze snel dood. Hun zieke tegenhangers gedragen zich echter heel anders – tumoren groeien snel en overtreffen vaak hun beschikbare zuurstofvoorraad, maar vertragen niet vanwege hun adaptieve aard; in plaats daarvan gedijen ze onder dergelijke omstandigheden zonder te stikken.
Kort daarna schakelen de kankercellen hun stofwisselingsproces over op zuurstofafhankelijke glycolyse. Ze beginnen overvloedige hoeveelheden melkzuur te produceren en af te voeren buiten de celgrenzen, waardoor de zure omstandigheden in de tumoromgeving toenemen.
Een verhoogde zuurgraad van dergelijke kankeromgevingen bevordert verdere penetratie en verspreiding door de extracellulaire matrix die de cellen van ons lichaam met elkaar verbindt af te breken. Wanneer deze zuurgraad escaleert, helpt het kwaadaardige gezwellen om ons immuniteitsmechanisme te omzeilen – een inherente bescherming tegen ziektes zoals deze. Dit is ontegenzeggelijk een van de redenen waarom immuuntherapie vaak de neiging heeft om zijn effect te verliezen bij gevorderde stadia van kanker.
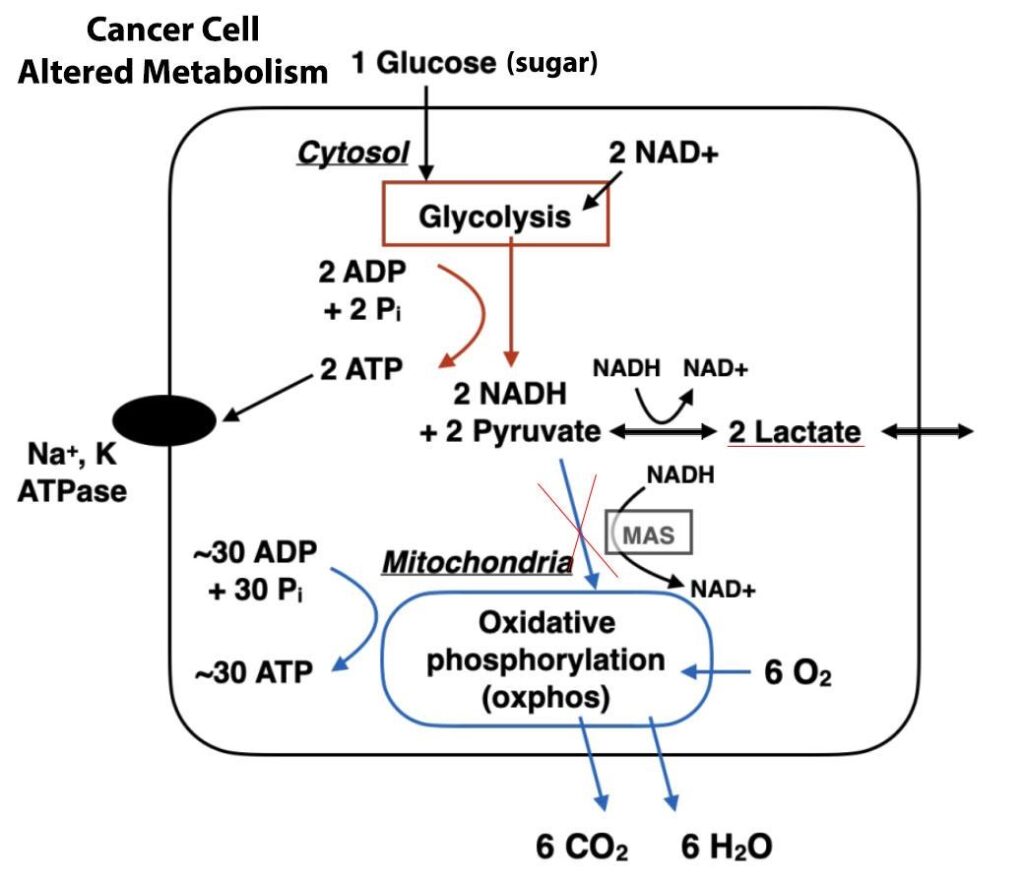
Tegelijkertijd verbruiken kankercellen minder zuurstof, waardoor de mitochondriën in de cellen minder reactieve zuurstofspecies genereren. Deze spelen een cruciale rol bij het stoppen en verwijderen van schadelijke kankercellen. De ziekte begint een mechanisme te ontwijken dat apoptose wordt genoemd.
Apoptose is een gewoon fenomeen dat in ons lichaam optreedt; het verwijdert op een handige manier ongewenste of overtollige cellen uit het voortbestaan van de anatomie.
Het is in wezen een natuurlijke, van tevoren geregelde celdood die tumorgroei bij aanvang stopt door zichzelf uit te roeien, in de eerste plaats om mogelijke onnodige uitbreiding van deze tumoren in ons te voorkomen, waardoor onherstelbare schade wordt aangericht en kwaadaardige cellichamen onherstelbaar worden.
Dit zijn belangrijke metabolische voordelen die ongereguleerde progressie van de levenscyclus van verschillende transformaties mogelijk maken, terwijl ze voor onbepaalde tijd onsterfelijk blijven door het afschrikken van geprogrammeerde tijdige sterfte (apoptose).
Een belangrijke vermelding gaat namelijk naar dit nogal ingewikkelde evolutieproces dat neoplastische metamorfosen ondergaan en dat beoefenaars uitdaagt om van dergelijke kwalen geduchte tegenstanders te maken die complexe behandelingsprotocollen vereisen, maar laten we ook een ander aspect niet vergeten, namelijk de hefboomwerking van het Warburg-effect tegen kankerverwekkende stoffen.
Bij het opsporen van ziekten heeft de mensheid gebruik gemaakt van dit verschijnsel van het kankermetabolisme. De test die bekend staat als positronemissietomografie (PET) brengt weefsels en organen met ongewone metabolische activiteit in beeld.
Omdat kankercellen het Warburg-effect vertonen, absorberen ze radioactief glucose met een snelheid die honderden malen hoger is dan die van standaardweefsel eromheen. Als gevolg hiervan worden tumoren verlicht op de resulterende beelden, waardoor ze gemakkelijk door het hele lichaam kunnen worden gevolgd.
Wat de behandeling betreft: als we erkennen dat bijna alle eerdere behandelingen tegen kanker zich uitsluitend richtten op technieken waarbij het gen centraal stond, zou de ‘Warburg’-paradigmaverschuiving mogelijk gezien kunnen worden als een over het hoofd geziene ‘achilleshiel’ in elke benadering die gericht is op de behandeling van kanker over een periode van bijna een eeuw. Een alternatieve verbinding – natriumdichlooracetaat (DCA) werkt op unieke wijze door abnormale celfuncties met betrekking tot de stofwisseling weer in evenwicht te brengen.
Noodzaak voor immunotherapie
Kankercellen hebben verschillende mechanismen ontwikkeld om zichzelf te camoufleren, waardoor ze niet gedetecteerd worden door het immuunsysteem van ons lichaam. Ze kunnen genetische mutaties hebben of verschillende oppervlakte-eiwitten vertonen – beide factoren kunnen het immuunsysteem verhinderen om deze cellen te onderscheiden en te bestrijden.
Dit is waar TIL’s een integraal onderdeel van uitmaken in dit scenario. Als de tumoren van een patiënt niet uit deze TIL’s bestaan, betekent dit dat de afweerreactie niet effectief is in de strijd tegen de kwaadaardigheid, waardoor een immunotherapeutische interventie nodig is.
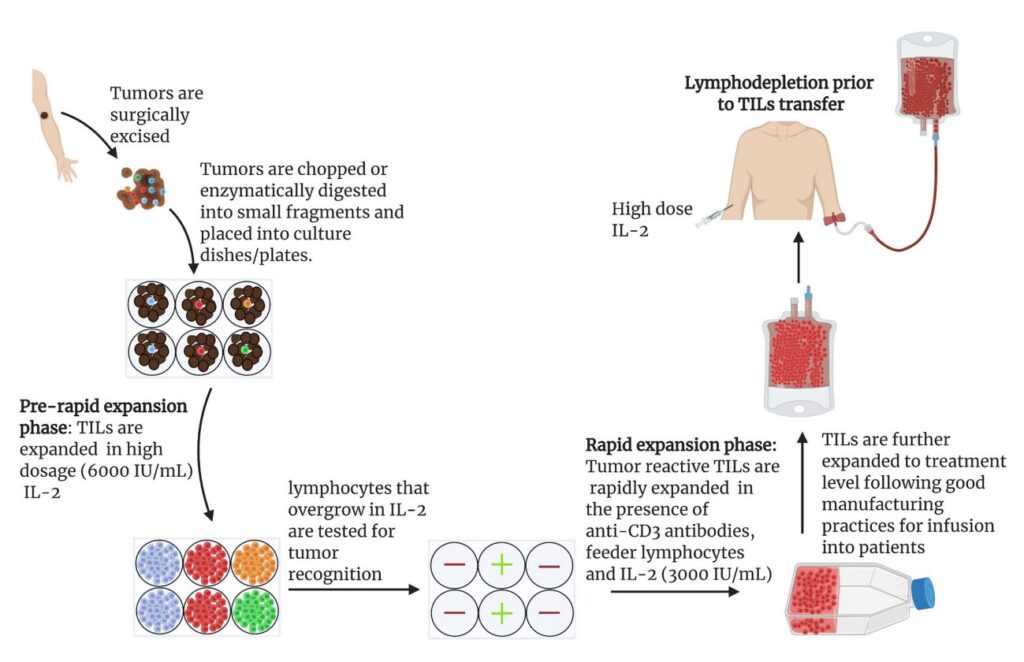
Problemen met immunotherapie bij kanker
De behandeling van kanker is een nieuwe fase ingegaan met immunotherapie, wat veel mensen optimistisch stemt. Toch is deze aanpak niet zonder complicaties. Een belangrijk punt van zorg is het vermogen van kankercellen om na verloop van tijd tolerantie op te bouwen. Door hun hoge energieproductie via het glycolyseproces blokkeren deze schadelijke cellen vaak specifieke routes die belangrijk zijn voor het effectief aansturen van de functies van T-cellen.
Als deze T-cellen niet goed zijn gerijpt, slagen ze er niet in om tumorcellen te identificeren en efficiënt te neutraliseren, waardoor ze in plaats daarvan worden gestimuleerd door de kracht die ze eerder hebben opgedaan met de therapeutische antilichamen die ze eerder hebben gekregen.
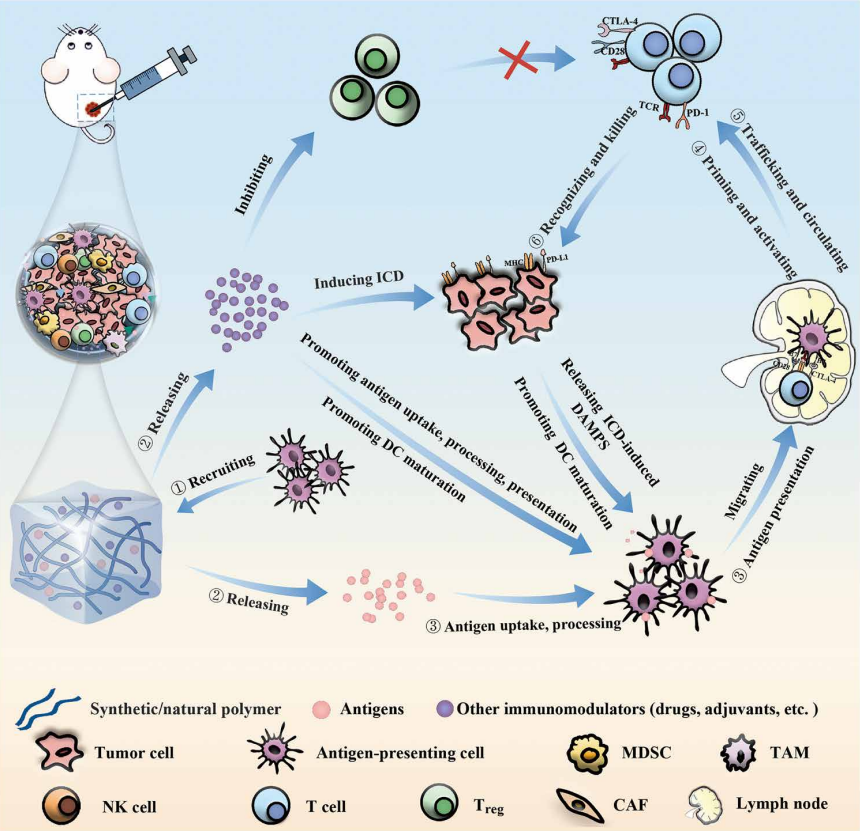
De problemen aanpakken
Als antwoord op deze hindernissen zou het voordelig kunnen zijn om de inspanningen te richten op het remmen van het energieproductiesysteem van tumorcellen na immuuntherapie. Door hun energievoorziening te beperken, zouden ze mogelijk niet in staat zijn om signaalpaden te blokkeren die de ontwikkeling en controle van T-cellen bepalen.
Laatste bevindingen in wetenschappelijke onderzoeken: 2-deoxy-D-glucose (2DG)
In de behandeling van kanker, vooral voor Triple Negative Breast Cancer (TNBC), is er een opwindende ontwikkeling.
Wetenschappers hebben ontdekt dat het combineren van immuuntherapie met een glucose antimetaboliet bekend als 2DG de effectiviteit van de behandeling zou kunnen verbeteren. Dit is vooral opmerkelijk omdat TNBC-cellen vaak hoge niveaus vertonen van een eiwit met de naam geprogrammeerd dood-ligand 1 (PD-L1).
Het probleem met de behandeling van TNBC is dat slechts een kleine groep patiënten, ruwweg 10 tot 20%, daadwerkelijk positieve resultaten ziet van therapieën die zich richten op PD-L1 of PD-1, belangrijke spelers in de immuunrespons van het lichaam.
Deze nieuwe benadering met 2DG zou het spel kunnen veranderen voor veel TNBC-patiënten die momenteel beperkte behandelingsresultaten hebben.
Hier is een belangrijk punt: een bepaalde vorm van PD-L1, bekend als geglycosyleerd PD-L1, is cruciaal voor de interacties die plaatsvinden binnen het PD-L1-PD-1 raamwerk. Bovendien hebben cellen die geassocieerd worden met TNBC vaak hogere niveaus van deze geglycosyleerde PD-L1 in vergelijking met niet-TNBC-cellen.
Onderzoek heeft aangetoond dat door de stabiliteit en functie van deze immuunremmende pro-kankermolecule aanzienlijk te beïnvloeden, de hoeveelheid glycosylering op PD-L1 kan worden verminderd.
Dit is waar “deoxyglucose” om de hoek komt kijken. Het gebruik van deoxyglucose kan dit proces mogelijk verstoren, wat kan leiden tot nieuwe strategieën die verschillende benaderingen combineren voor effectievere resultaten bij de behandeling van TNBC.
Technieken voor kankerbehandeling: Conventionele en progressieve methoden
De reis naar doeltreffende oplossingen voor kanker omvat talrijke methoden, van conventionele tot meer avant-gardistische technieken.
Gevestigde behandelingsprocedures zoals chemotherapie en radiotherapie worden alom erkend, terwijl nieuwe elementen zoals 2DG steeds aantrekkelijker zijn geworden vanwege hun mogelijke voordelen bij de behandeling van kanker, hetzij afzonderlijk of in combinatie met gevestigde hulpmiddelen zoals fenbendazol en DCA die ook aanzienlijk bijdragen aan de bestrijding van de ziekte.

Chemotherapie
Het gebruik van chemotherapie is nog steeds een cruciaal element in de strijd tegen de ziekte die kanker heet. Het is vooral effectief bij aandoeningen zoals borstkanker, waar het wordt gebruikt om de grootte van de tumor te verkleinen en chirurgische verwijdering te vergemakkelijken – een aanpak die preoperatieve chemotherapie of PCT wordt genoemd.
Maar ook al worden de tumoren kleiner, we kunnen niet altijd alleen op deze methode vertrouwen omdat er veel gevallen zijn waarin de kwaadaardige cellen na de behandeling weer verschijnen.
Het effect van chemotherapie verbeteren met 2DG
Studies wijzen uit dat het verweven van chemotherapie met 2DG de effectiviteit ervan kan versterken. 2DG, dat functioneel op glucose lijkt, is in staat om in te grijpen in de metabolische activiteiten binnen kankercellen en dit zou mogelijk het effect van reguliere chemotherapiebehandelingen kunnen vergroten.
Het dubbele gebruik symboliseert het potentieel voor een uitgebreide pathologische respons, wat betekent dat sterkere en langdurigere behandelingsresultaten haalbaar zijn. Er zijn talrijke laboratoriumtests en dierstudies uitgevoerd om deze gecombineerde strategie te bevestigen.
Bestralingstherapie
Binnen kankercellen is 2DG de op zichzelf staande methode om de suikerstofwisseling te reguleren, maar het wordt ook gecombineerd met therapievormen zoals chemotherapie en radiotherapie.
Realistisch gezien speelt radiotherapie een cruciale rol bij de behandeling van kanker. Ongeveer 60% van de mensen die tegen deze wrede ziekte vechten, zullen dit type behandeling alleen of in combinatie met andere behandelingen ondergaan.
Hoewel radiotherapie een krachtig hulpmiddel is in de strijd tegen kanker, is het niet zonder uitdagingen. Het is ongetwijfeld effectief, maar het kan na verloop van tijd een aantal ongewenste bijwerkingen hebben. Een grote zorg is dat kankercellen een resistentie tegen de straling kunnen ontwikkelen en er is ook een risico op beschadiging van gezonde cellen.
Om deze problemen aan te pakken, vooral het probleem van stralingstolerantie, is het cruciaal om glycolytische remmers in te zetten. Deze remmers werken door de energietoevoer naar de kankercellen af te snijden, waardoor ze in wezen uitgehongerd raken van de voedingsstoffen die ze nodig hebben.
Dit maakt het moeilijker voor deze kankercellen om zichzelf te herstellen nadat ze zijn getroffen door straling, wat leidt tot hun uiteindelijke afbraak en vernietiging. Een dergelijke aanpak is een stap voorwaarts om bestralingstherapie veiliger en effectiever te maken voor patiënten.
Versterking van radiotherapie met 2-Deoxy-D-Glucose
2DG is een instrumentele glycolytische remmer. De functie bestaat uit het binden aan het glucosetransportereiwit GLUT1 voordat het gefosforyleerd wordt door het enzym Hexokinase. Daar eindigt echter de metabole progressie, waardoor de glycolytische route geblokkeerd blijft.
Kankercellen die aan deze remmer worden blootgesteld, slagen er dus niet in energie te produceren doordat het normale glycolyseproces van glucose wordt onderbroken. Daarnaast zet 2DG caspase 3 en PARP enzymen aan tot apoptose in kwaadaardige cellen, terwijl gezonde cellen ongemoeid worden gelaten.
Voor de behandeling van kanker ligt er een veelbelovende combinatie in het verschiet: 2-deoxy-D-glucose (2DG) in combinatie met radiotherapie. Dit duo zou de kracht van bestralingstherapie aanzienlijk kunnen vergroten. Hoe?
2DG werkt als een glucoseremmer. Het belemmert het vermogen van kankercellen om zichzelf te herstellen nadat ze zijn beschadigd door bestraling, voornamelijk omdat deze cellen uitgehongerd zijn van glucose en essentiële voedingsstoffen.
Maar 2DG is niet zomaar een eendagsvlieg. Het dient meerdere doelen. Behalve dat het een verstoorder is, versterkt het ook de impact van bestraling. De werking is gekoppeld aan het veranderen van het evenwicht van oxidatiereductieprocessen in cellen.
Een belangrijk aspect om op te merken is dat oxidatieve stress verondersteld wordt een sleutelroute te zijn waardoor ioniserende straling kankercellen doodt. Deze nieuwe benadering, waarbij 2DG wordt gebruikt in combinatie met radiotherapie, zou een doorbraak kunnen betekenen in de effectieve behandeling van kanker.
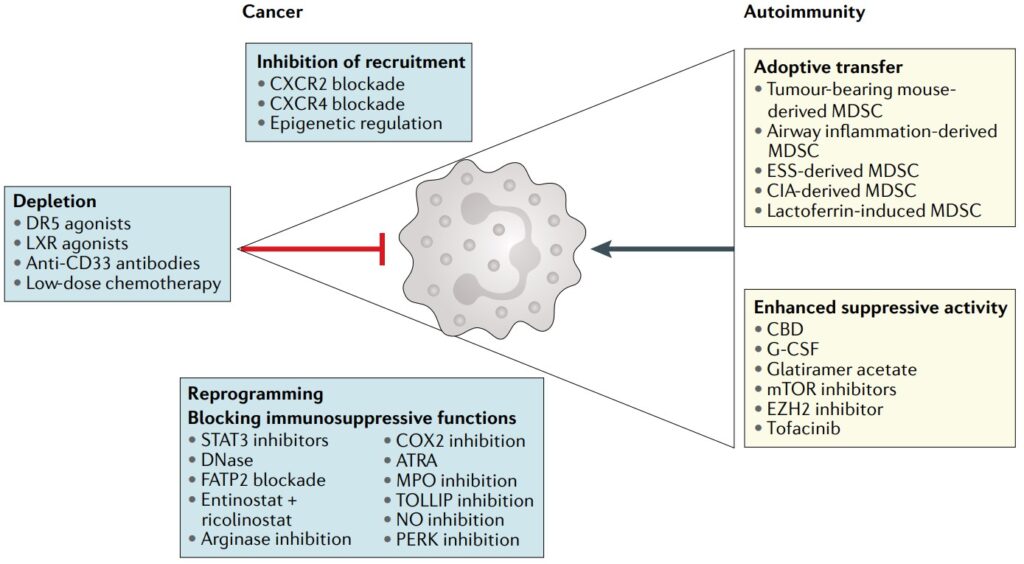
Diversiteit van kankercellen
Kankercellen zijn divers, iets wat wetenschappers tumorheterogeniteit noemen, en het is iets wat je in bijna elke kankersoort aantreft. Deze diversiteit komt vaak voort uit fouten die gemaakt worden tijdens het DNA replicatieproces wanneer cellen zich delen.
Dit is wat er gebeurt: Als cellen zich delen en er fouten worden gemaakt bij het kopiëren van hun DNA, ontstaan er nieuwe cellen met mutaties. Na verloop van tijd, vooral als bepaalde omgevingsfactoren als triggers fungeren, kunnen deze gemuteerde cellen evolueren en mogelijk leiden tot kanker. Het is een langzaam proces, maar het is hoe veel kankers hun reis beginnen.
Verschillende vormen van kankerongelijkheid
De differentiatie die wordt waargenomen bij kankercellen, ook wel tumor heterogeniteit genoemd, kan eenvoudigweg worden verdeeld in twee divisies:
Spatiale tumor heterogeniteit
Dit betekent dat kankercellen zich niet gelijkmatig over het aangetaste weefsel verspreiden. In plaats daarvan hebben ze de neiging om zich lukraak en onvoorspelbaar te verspreiden.
Tijdlijnfluctuaties in tumordiversiteit
Als tumoren zich in de loop van de tijd ontwikkelen, evolueren ze vaak in verschillende subtypen. Dit proces staat bekend als temporele heterogeniteit. Het komt erop neer dat hoe langer een tumor groeit, hoe gevarieerder hij kan worden.
De uiteenlopende eigenschappen van tumorcellen vormen een belangrijk obstakel bij het effectief bestrijden van kanker. De uiteenlopende aard van deze kwaadaardige cellen resulteert vaak in resistentie tegen de huidige therapeutische strategieën.
Gezien deze complexiteit in het gedrag van kankercellen is er een dringende behoefte om behandelingen te ontwikkelen die zich effectief kunnen richten op de resistentie die wordt veroorzaakt door de gevarieerde genetische samenstelling van individuele kankercellen.
Testresultaten
Een breed scala aan onderzoeken, waaronder laboratoriumtests, dierstudies en klinische studies bij mensen, hebben een diepe duik genomen in de effecten van 2-deoxy-D-glucose (2DG) op cellen. Wat uit dit onderzoek naar voren komt, is dat 2DG op een complexe manier werkt.
Het stopt niet alleen het proces van cellulaire glycolyse; het bevordert ook apoptose, of geprogrammeerde celdood, zonder gezonde cellen te beschadigen. Bovendien heeft 2DG invloed op hoe genen zich gedragen in cellen.
Het verstoort transcriptiefactoren die essentieel zijn voor het activeren van genen die essentieel zijn voor celreplicatie. Dit inzicht wijst op het potentieel van 2DG als wapen tegen verschillende kenmerken van kankercellen.
Eén ding dat moet worden opgemerkt over kankercellen is hun verscheidenheid aan genetische mutaties, die een rol spelen in de progressie van de ziekte. Ze hebben echter allemaal één ding gemeen: een hogere snelheid van suikermetabolisme vergeleken met normale cellen.
Dit maakt 2DG een potentieel effectieve behandeling voor een verscheidenheid aan kankers. Het werkt door de kankercellen uit te hongeren van suiker en zuurstof, terwijl het ook hun genactiviteit beïnvloedt. Deze aanpak kan de celgroei vertragen en sturen in de richting van zelfvernietiging, waardoor overmatige groei wordt voorkomen.
Prospectieve genezing voor glioblastoomkanker
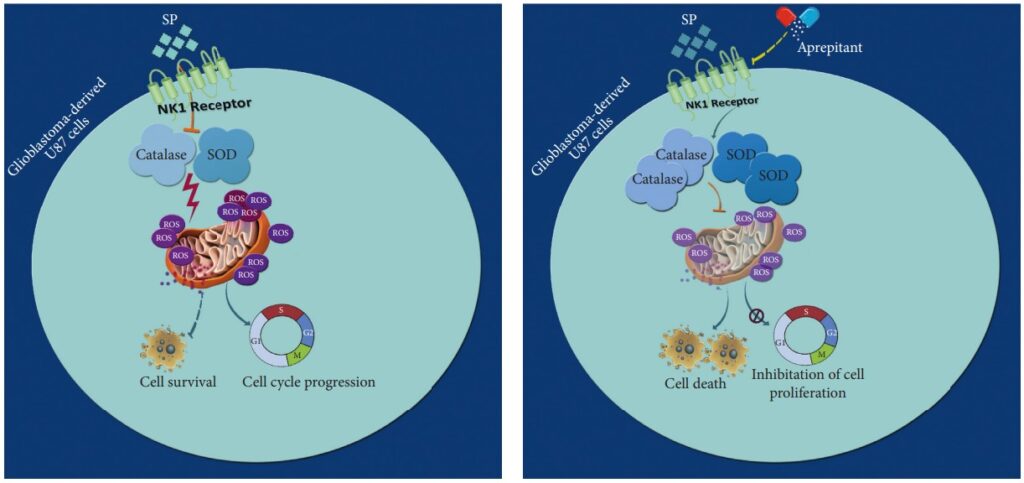
Glioblastoom onderscheidt zich als een bijzonder agressieve vorm van hersenkanker, die bekend staat om zijn sterke resistentie tegen celdood en het beperkte succes van de huidige behandelingen. Deze situatie onderstreept de dringende noodzaak om nieuwe behandelingsmogelijkheden te onderzoeken.
Nog niet zo lang geleden begonnen Dr. Evangelos Michelakis, een toegewijd medisch wetenschapper, en zijn team aan verschillende onderzoeksprojecten gericht op de behandeling van Glioblastoma multiforme (GBM). Ze realiseerden zich dat een ideale behandeling de bloed-hersenbarrière zou moeten kunnen passeren en zich specifiek zou moeten richten op kankercellen, zonder gezond weefsel te beschadigen.
Hun keuze, natriumdichlooracetaat (DCA), vertoonde deze kwaliteiten en, nog belangrijker, vertoonde geen tekenen van schade aan het bloed, hart, nieren of lever.
Deze ontdekking leidde tot een baanbrekend onderzoek met echte patiënten, dat de weg vrijmaakte voor verdere baanbrekende bevindingen in de behandeling van GBM.
Invloed van DCA op het afsterven van kankercellen en de ontwikkeling van tumoren
Het wordt duidelijk dat dichlooracetaat (DCA) een grote invloed heeft op de bestrijding van kanker, vooral in het geval van Glioblastoma, een dodelijke vorm van hersenkanker. DCA heeft het vermogen om de dood van kankercellen te induceren, de bloedvaten die tumoren voeden te verkleinen en de groei van deze agressieve vorm van kanker te vertragen.
Wat vooral veelbelovend is, is dat DCA misschien wel het meest effectief is als het naast andere behandelingen wordt gebruikt, wat een nieuw sprankje hoop biedt in de strijd tegen deze uitdagende ziekte.
Naast andere behandelingen voor glioblastoom
In een zeldzame gelegenheid kregen wetenschappers de kans om hersenweefsel van patiënten te vergelijken voor en na hun behandeling met DCA. Wat ze zagen was bemoedigend: een afname van kankercellen in het hersenweefsel na de behandeling.
Dit werd toegeschreven aan een toename in de vernietiging van dodelijke cellen en een afname in de groei van kwaadaardige glioblastoma multiforme cellen. Het onderzoek concludeerde dat het combineren van DCA met andere behandelingen een effectieve strategie tegen GBM zou kunnen zijn.
Het onderzoeksteam stelt voor om dichlooracetaat, dat bekend staat als niet-toxisch, te gebruiken voor of na procedures zoals radiotherapie of chirurgie. Deze aanpak zou de voordelen van standaardbehandelingen voor GBM kunnen vergroten.