Dr. Gregory Riggins, professor i neurokirurgi och onkologi vid Johns Hopkins, och hans forskargrupp stöter vanligtvis på små eller inga svårigheter när det gäller att få cancer att växa i testmöss för deras studier.
Under en period på flera månader 2009 fanns det dock ett kluster av dessa möss där tumörutvecklingen helt enkelt inte ville komma igång. Efter ytterligare undersökningar upptäckte de att detta oväntade resultat berodde på att dessa gnagare hade administrerats fenbendazol som en antiparasitär behandling.
”När vi undersökte olika läkemedel inom denna grupp visade sig fenbendazol vara det mest effektiva. Detta väckte vår uppmärksamhet.” Sa forskaren
När nyheten om fenbendazolets förmåga började spridas upptäckte man att det kunde administreras ensamt eller i kombination med andra metoder för att bota eller hindra cancertillväxt.
Riggins och Gallia inledde tillsammans med sin forskargrupp en plan för att inte bara förstå hur detta läkemedel fungerar utan också förbättra dess användbarhet mot glioblastomceller och få det producerat för patientförsök. Enligt dessa forskares övertygelse bidrar fenbendazol till att blockera tumörutvecklingen genom att hindra bildandet av tubulinsträngar – proteiner som är avgörande för cancercellernas tillväxt.
Denna händelse inträffade för över ett decennium sedan. Nu har det gått lång tid och vi har fått betydande kunskaper om hur fenben kan användas effektivt för att öka sannolikheten för att vi ska kunna utrota cancer.
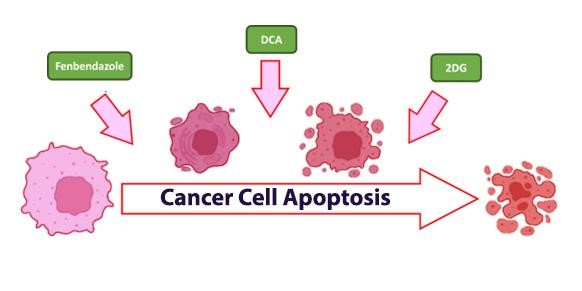
Cancerns energistruktur
År 1923 presenterade Otto Heinrich Warburg – en viktig tysk biokemist, praktiserande läkare och mottagare av Nobelpriset – en ovärderlig upptäckt som spelade en viktig roll i förståelsen av cancercellernas energiomsättningsmönster. Detta speciella observerade fenomen är för närvarande erkänt som den viktigaste egenskapen hos cancer som kallas mer allmänt kallad ”Warburg-effekten.”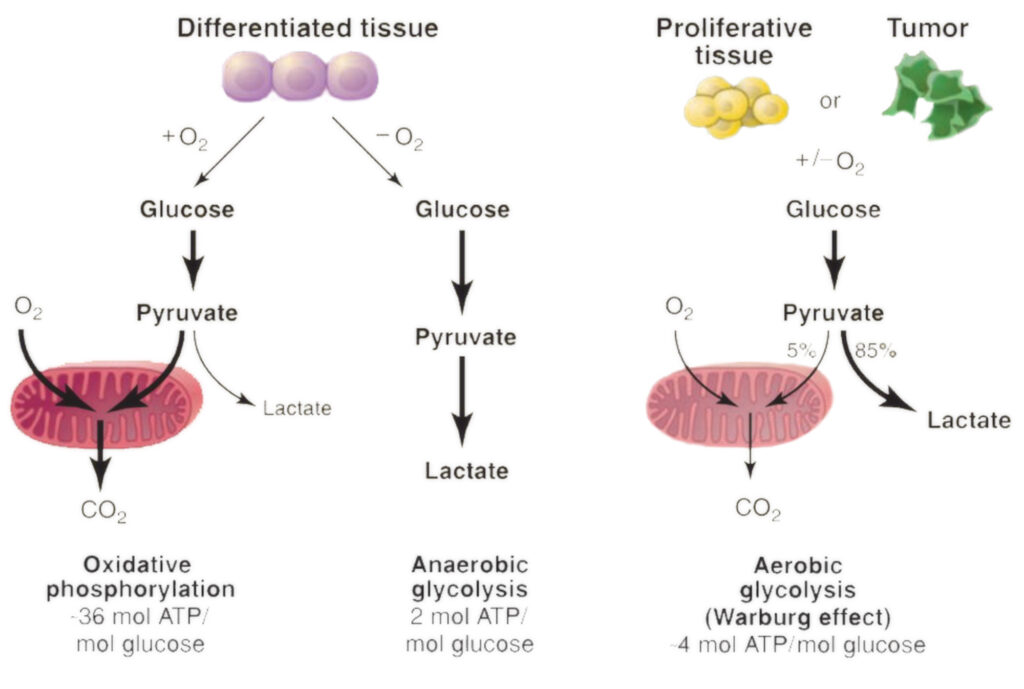
En anmärkningsvärd observation som Warburg gjorde var när han studerade tumörceller från råtta: han noterade att de blomstrade på exceptionellt höga nivåer av glukos (socker) istället för att öka användningen av syre för tillväxtändamål, vilket verkade kontraintuitivt eftersom utvinning av energi från näringsämnen via högre utnyttjandegrad av syre skulle ha varit en i stort sett effektiv process.
Upptäckten av sådana resultat under dessa tider för cirka hundra år sedan väckte stor nyfikenhet som ledde till obesvarade frågor än lösningar som fanns tillgängliga till hands.
Det stora glukosbehovet och den minskade syreförbrukningen ger cancercellerna en tydlig uppsättning evolutionära fördelar. Ett sätt på vilket Warburgpåverkan hjälper elakartade celler är genom att underlätta snabb ackumulering av biomassa. Det förbättrade glukosupptaget förser tumörvävnaden med överflödiga byggstenar för att skapa nytt genetiskt material och protein, vilket leder till en ökning av både spridningen och expansionen av cancer.
Dessutom är det ingen hemlighet att normala däggdjursceller kräver ett konstant flöde av syre, annars dör de snabbt. Deras sjuka motsvarigheter beter sig dock helt annorlunda – tumörer växer snabbt och överskrider ofta deras tillgängliga syreförsörjning men saktar inte ner på grund av sin adaptiva natur; istället trivs de under sådana omständigheter utan att kvävas.
Inom kort ställer cancercellerna om sin metaboliska process till syreberoende glykolys. De börjar generera och släppa ut rikliga mängder mjölksyra utanför cellgränserna, vilket leder till en ökning av sura förhållanden i tumörens omgivning.
Ökad syrahalt i sådana cancermiljöer främjar ytterligare penetration och spridning genom att bryta ned kroppens cellbindande extracellulära matrix. När denna syranivå eskalerar hjälper den elakartade tumören att kringgå vår immunitetsmekanism – ett inbyggt skydd mot sjukdomar som dessa. Det är onekligen en anledning till att immunterapi ofta tenderar att förlora sin effekt när man arbetar med avancerade cancerstadier.
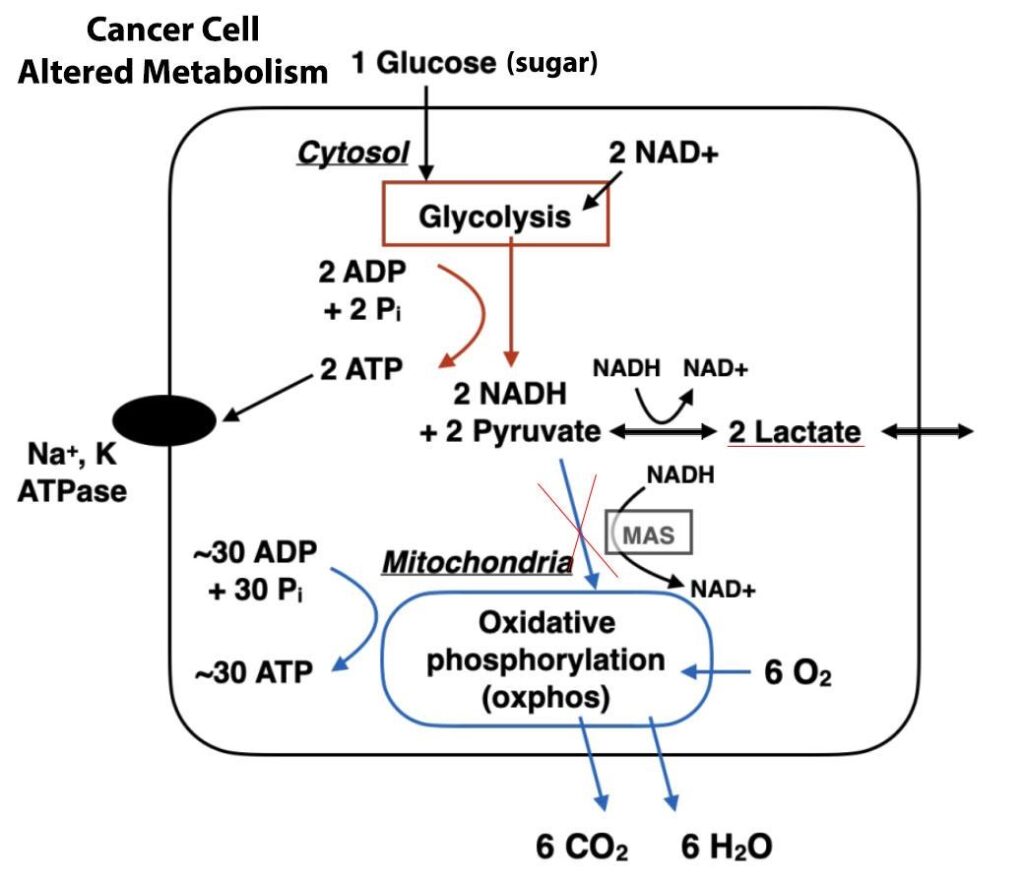
Samtidigt förbrukar cancercellerna mindre syre, vilket leder till att mitokondrierna i dem genererar färre reaktiva syreföreningar. Dessa har en avgörande funktion för att både stoppa och ta bort skadliga cancerceller. Sjukdomen börjar undvika en mekanism som kallas apoptos.
Apoptos är ett vanligt fenomen som förekommer i vår kropp; det tar enkelt bort oönskade eller överdrivna celler från att fortsätta sin existens med anatomin.
Det är i huvudsak naturlig förutbestämd cellulär död som stoppar tumörtillväxt i början genom att utrota sig själv främst för att förhindra eventuell onödig expansion av dessa tumörer inuti oss som orsakar skador bortom reparation, vilket gör maligna cellkroppar oändliga.
Detta är viktiga metaboliska fördelar som möjliggör oreglerad livscykelutveckling av olika transformationer samtidigt som de blomstrar på obestämd tid och är odödliga på grund av att de förhindrar programmerad död i rätt tid (apoptos).
Ett viktigt omnämnande går nämligen till denna ganska invecklade utvecklingsprocess som neoplastiska metamorfoser genomgår, vilket tenderar att utmana utövare som gör sådana sjukdomar till formidabla motståndare som kräver komplexa behandlingsprotokoll, men låt oss inte heller glömma en annan aspekt, dvs. att utnyttja Warburg-effekten mot cancerframkallande ämnen.
När det gäller att identifiera sjukdomar har mänskligheten utnyttjat denna förekomst av cancermetabolism för detektionsändamål. Det test som kallas positronemissionstomografi (PET) visar vävnader och organ med ovanlig metabolisk aktivitet.
Eftersom cancerceller uppvisar Warburg-effekten absorberar de radioaktivt glukos i en hastighet som är hundratals gånger högre än standardvävnaden runt omkring dem. Följaktligen blir tumörerna belysta i de resulterande bilderna, vilket gör det enkelt att spåra dem genom hela kroppen.
När det gäller behandling skulle ett erkännande av att nästan alla tidigare cancerbehandlingar enbart fokuserade på gencentrerade tekniker kunna leda till att paradigmskiftet ”Warburg” potentiellt ses som en förbisedd ”akilleshäl” i alla metoder som inriktats på att behandla cancer under nästan ett sekels tid. En alternativ förening – natriumdikloracetat (DCA) fungerar unikt genom att återställa onormala cellfunktioner relaterade till metabolism tillbaka till jämvikt
Nödvändigheten av immunterapi
Cancerceller har utvecklat olika mekanismer för att kamouflera sig så att de inte kan upptäckas av kroppens immunförsvar. De kan ha genetiska mutationer eller tydliga ytproteiner – båda faktorerna kan hindra immunsystemet från att urskilja och bekämpa dessa celler.
Det är här TIL är en viktig del i detta scenario. Om en patients tumörer inte består av dessa TIL-celler innebär det att det defensiva immunförsvaret inte effektivt bekämpar maligniteten, vilket kräver en immunterapeutisk intervention.
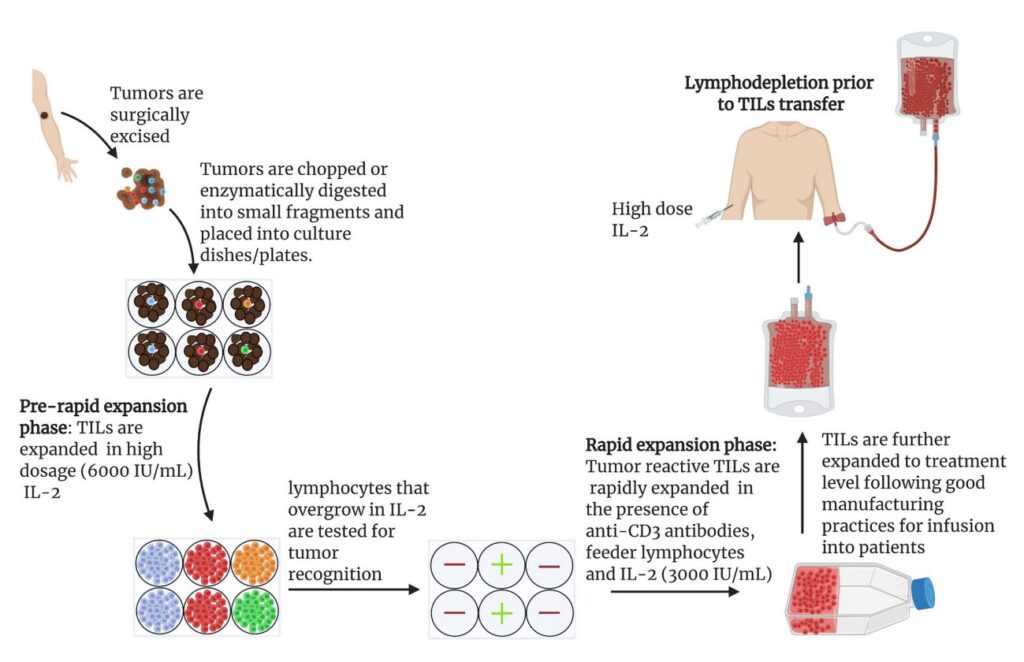
Svårigheter med immunterapi mot cancer
Cancerbehandlingen har gått in i en ny fas med immunterapi, vilket inger optimism hos många människor. Denna metod är dock inte utan komplikationer. Ett stort bekymmer är cancercellernas förmåga att bygga tolerans över tid. På grund av sin höga energiproduktion via glykolys blockerar dessa skadliga celler ofta specifika vägar som är viktiga för att hantera T-cellernas funktioner på ett effektivt sätt.
Om dessa T-celler inte mognar korrekt kan de inte framgångsrikt identifiera och neutralisera tumörceller på ett effektivt sätt, vilket gör att de i stället främjas av den tidigare styrkan från de terapeutiska antikroppar som tidigare givits.
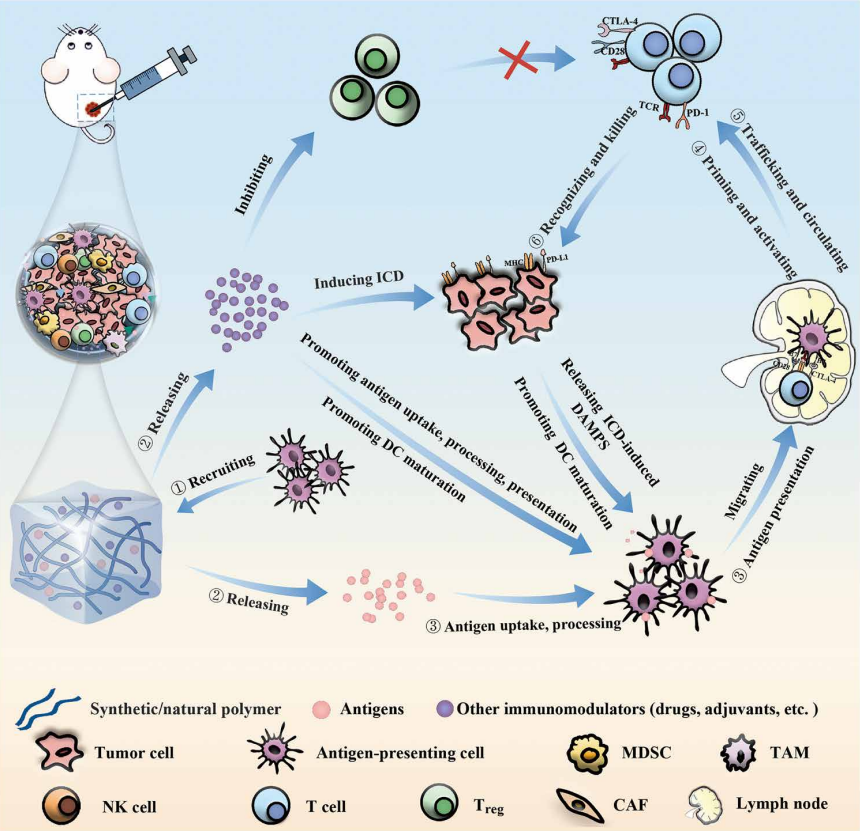
Ta itu med svårigheterna
Som svar på dessa hinder skulle det kunna vara fördelaktigt att rikta in sig på att hämma tumörcellernas energiproduktionssystem efter immunterapi. Genom att begränsa deras energiförsörjning finns det en potential att de inte skulle kunna blockera signalvägar som dikterar T-cellernas utveckling och kontroll.
De senaste rönen från vetenskapliga studier: 2-deoxy-D-glukos (2DG)
Inom cancerbehandling, särskilt för trippelnegativ bröstcancer (TNBC), har det skett en spännande utveckling.
Forskare har upptäckt att en kombination av immunterapi och en glukosantimetabolit som kallas 2DG kan förbättra behandlingens effektivitet. Detta är särskilt anmärkningsvärt eftersom TNBC-celler ofta uppvisar höga nivåer av ett protein som kallas programmerad dödsligand 1 (PD-L1).
Problemet med behandling av TNBC är att endast en liten grupp patienter, cirka 10-20 procent, faktiskt får positiva resultat av behandlingar som är inriktade på PD-L1 eller PD-1, vilka är viktiga aktörer i kroppens immunförsvar.
Den nya metoden med 2DG kan potentiellt förändra spelplanen för många TNBC-patienter som för närvarande har begränsade behandlingssvar.
Här är en viktig punkt: en särskild form av PD-L1, som kallas glykosylerad PD-L1, är avgörande för de interaktioner som äger rum inom ramen för PD-L1-PD-1. Dessutom tenderar celler med TNBC att ha högre nivåer av detta glykosylerade PD-L1 jämfört med icke-TNBC-celler.
Forskning har visat att man kan minska mängden glykosylering på PD-L1 genom att avsevärt påverka stabiliteten och funktionen hos denna immunhämmande pro-cancermolekyl.
Det är här som ”deoxiglukos” kommer in i bilden. Användning av deoxiglukos kan potentiellt störa denna process, vilket kan leda till nya strategier som kombinerar olika tillvägagångssätt för effektivare behandlingsresultat vid TNBC.
Tekniker för cancerbehandling: Konventionella och progressiva metoder
På vägen mot effektiva cancerlösningar används många olika metoder, från konventionella till mer avancerade tekniker.
Etablerade behandlingsmetoder som kemoterapi och strålbehandling är allmänt erkända, medan nya element som 2DG har blivit alltmer attraktiva på grund av deras potentiella fördelar vid behandling av cancer, antingen enskilt eller tillsammans med väletablerade hjälpmedel som fenbendazol och DCA som också bidrar väsentligt till att bekämpa sjukdomen.

Kemoterapi
Kemoterapi är fortfarande en viktig del i kampen mot den sjukdom som kallas cancer. Den är särskilt effektiv vid tillstånd som bröstcancer, där den används för att minimera tumörstorleken och underlätta kirurgiskt avlägsnande – en metod som kallas preoperativ kemoterapi eller PCT.
Men även om det kan minska tumörens storlek kan vi inte alltid förlita oss enbart på denna metod eftersom det finns många fall där de maligna cellerna återkommer efter behandlingen.
2DG förstärker effekten av kemoterapi
Studier visar att en kombination av kemoterapi och 2DG kan förstärka dess effektivitet. 2DG, som funktionellt liknar glukos, kan störa de metaboliska aktiviteterna i cancerceller och detta kan potentiellt öka effekten av vanliga kemoterapibehandlingar.
Den dubbla användningen symboliserar potentialen för en omfattande patologisk respons, vilket innebär att starkare och mer långvariga behandlingsresultat kan uppnås. Ett stort antal laboratorietester och djurstudier har utförts för att bekräfta denna kombinerade strategi.
Strålbehandling
I cancerceller är 2DG den fristående metoden för att reglera sockermetabolismen, men den kombineras också med terapiformer som kemoterapi och strålbehandling.
Realistiskt sett spelar strålbehandling en avgörande roll vid behandling av cancer. Cirka 60% av dem som kämpar mot denna grymma sjukdom kommer att uppleva denna typ av behandling antingen enskilt eller i samband med andra behandlingar.
Strålbehandling är visserligen ett kraftfullt verktyg i kampen mot cancer, men det finns också utmaningar. Den är utan tvekan effektiv, men med tiden kan den ge en del ovälkomna biverkningar. Ett stort problem är att cancercellerna kan utveckla resistens mot strålningen, och det finns också en risk för att friska celler skadas.
För att hantera dessa problem, särskilt problemet med strålningstolerans, är det viktigt att ta med glykolytiska hämmare i mixen. Dessa hämmare verkar genom att strypa energiförsörjningen till cancercellerna, så att de i princip inte får i sig de näringsämnen de behöver.
Detta gör det svårare för cancercellerna att reparera sig själva efter att ha utsatts för strålning, vilket leder till att de slutligen bryts ned och förstörs. En sådan metod är ett steg framåt för att göra strålbehandling säkrare och mer effektiv för patienterna.
Förstärkning av strålbehandling med 2-Deoxy-D-Glukos
2DG är en glykolytisk hämmare. Dess funktion är att binda till glukostransportproteinet GLUT1 innan det fosforyleras av enzymet hexokinas. Dess metaboliska progression slutar dock där, vilket säkerställer att den glykolytiska vägen förblir obstruerad.
Som sådana misslyckas cancerceller som utsätts för denna hämmare med att producera energi på grund av avbruten normal glukos glykolys process. Förutom detta stimulerar 2DG caspase 3 och PARP-enzymernas funktioner som leder till apoptos inom maligna celler medan friska celler lämnas opåverkade.
Inom cancerbehandling finns det en lovande kombination vid horisonten: 2-deoxy-D-glukos (2DG) i kombination med strålbehandling. Denna duo kan avsevärt öka effekten av strålterapi. Hur kommer det sig?
Jo, 2DG fungerar som en glukoshämmare. Det stör cancercellernas förmåga att reparera sig själva efter att ha skadats av strålning, främst eftersom dessa celler är svältfödda på glukos och viktiga näringsämnen.
Men 2DG är inte bara en enkelspårig ponny. Det tjänar flera syften. Förutom att vara en störande faktor förstärker den också effekten av strålbehandling. Dess verkan är knuten till att förändra balansen mellan oxidations-reduktionsprocesser i cellerna.
En viktig aspekt att notera är att oxidativ stress tros vara en viktig väg genom vilken joniserande strålning dödar cancerceller. Denna nya metod, där 2DG används i kombination med strålbehandling, skulle kunna förändra förutsättningarna för en effektiv cancerbehandling.
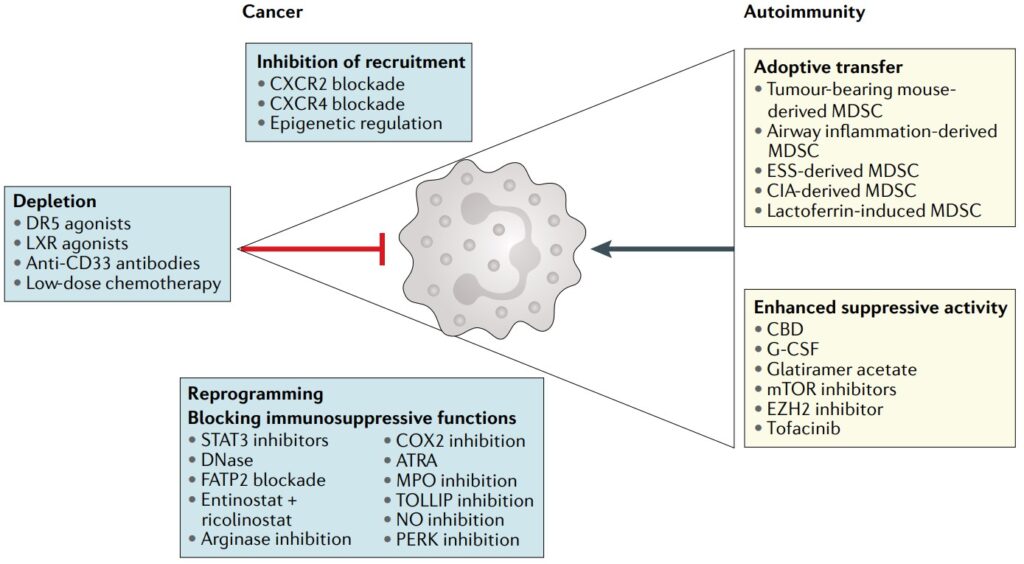
Cancercellernas mångfald
Cancerceller är en brokig skara, något som forskare kallar tumörheterogenitet, och det är något du hittar i nästan alla typer av cancer där ute. Denna mångfald beror ofta på misstag som begås under DNA-replikationsprocessen när cellerna delar sig.
Det här är vad som händer: När celler delar sig och det uppstår fel vid kopieringen av deras DNA, föds nya celler med mutationer. Med tiden, särskilt om vissa miljöfaktorer fungerar som utlösande faktorer, kan dessa muterade celler utvecklas och potentiellt leda till cancer. Det är en långsam process, men det är så många cancerformer börjar sin resa.
Olika former av skillnader i cancerförekomst
Den differentiering som observeras i cancerceller, och som kallas tumörheterogenitet, kan enkelt delas upp i två delar:
Spatiell tumörheterogenitet
Detta innebär att cancercellerna inte sprids jämnt över den drabbade vävnaden. Istället tenderar de att spridas på ett slumpmässigt och oförutsägbart sätt.
Tidsmässiga fluktuationer i tumördivergens
När tumörer utvecklas över tid utvecklas de ofta till olika undertyper. Denna process är känd som temporal heterogenitet. Ju längre en tumör växer, desto mer varierad kan den bli.
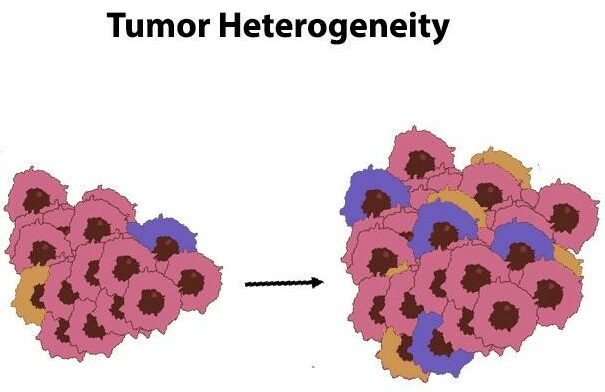
Tumörcellernas varierande egenskaper utgör betydande hinder när det gäller att effektivt bekämpa cancer. Dessa elakartade cellers varierande karaktär leder ofta till resistens mot nuvarande terapeutiska strategier.
Med tanke på komplexiteten i cancerbeteendet finns det ett stort behov av att utveckla behandlingar som effektivt kan riktas mot och övervinna den resistens som orsakas av den varierande genetiska sammansättning som finns i enskilda cancerceller.
Resultat av prövningen
Ett stort antal studier, inklusive laboratorietester, djurstudier och kliniska prövningar på människor, har gjort en djupdykning i effekterna av 2-deoxy-D-glukos (2DG) på celler. Det som framkommer av denna forskning är att 2DG fungerar på ett komplext sätt.
Det stoppar inte bara processen med cellulär glykolys, utan främjar även apoptos, eller programmerad celldöd, utan att skada friska celler. Dessutom påverkar 2DG hur generna beter sig i cellerna.
Det stör transkriptionsfaktorer som är viktiga för att aktivera gener som är nödvändiga för cellreplikation. Denna insikt pekar på potentialen hos 2DG som ett vapen mot olika egenskaper hos cancerceller.
En sak att notera när det gäller cancerceller är deras olika genetiska mutationer, som spelar en roll i sjukdomsförloppet. De tenderar dock alla att ha en sak gemensamt: en högre sockeromsättningshastighet jämfört med normala celler.
Detta gör 2DG till en potentiellt effektiv behandling av en rad olika cancerformer. Det verkar genom att svälta cancercellerna på socker och syre, samtidigt som det påverkar deras genaktivitet. Detta tillvägagångssätt kan bromsa celltillväxten och styra dem mot självdestruktion, vilket förhindrar överdriven tillväxt.
Prospektiv behandling av glioblastomcancer
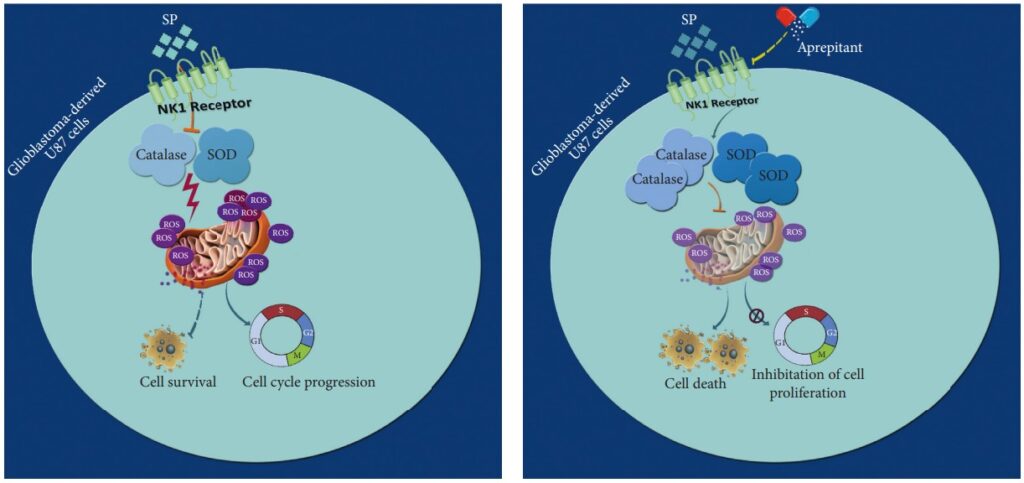
Glioblastom är en särskilt aggressiv form av hjärncancer, känd för sin starka motståndskraft mot celldöd och de nuvarande behandlingarnas begränsade framgång. Denna situation understryker det akuta behovet av att utforska nya behandlingsalternativ.
För inte så länge sedan inledde dr Evangelos Michelakis, en hängiven medicinsk forskare, och hans team flera forskningsprojekt med fokus på behandling av Glioblastoma multiforme (GBM). De insåg att en idealisk behandling måste kunna korsa blod-hjärnbarriären och rikta in sig specifikt på cancerceller, utan att skada frisk vävnad.
Deras val, natriumdikloracetat (DCA), hade dessa egenskaper och visade dessutom inga tecken på att orsaka skador på blod, hjärta, njurar eller lever.
Denna upptäckt ledde till att de genomförde en banbrytande studie med riktiga patienter, vilket banade väg för ytterligare banbrytande upptäckter vid behandling av GBM.
DCA:s inverkan på cancercellers nedbrytning och tumörutveckling
Det står alltmer klart att dikloracetat (DCA) har en betydande inverkan på cancerbekämpningen, särskilt när det gäller glioblastom, en dödlig form av hjärncancer. DCA har förmågan att få cancerceller att dö, minska de blodkärl som försörjer tumörerna och bromsa tillväxten av denna aggressiva cancerform.
Det som är särskilt lovande är att DCA kan vara mest effektivt när det används tillsammans med andra behandlingar, vilket ger en ny strimma av hopp i kampen mot denna utmanande sjukdom.
Tillsammans med andra behandlingar av glioblastom
Vid ett sällsynt tillfälle fick forskarna chansen att jämföra hjärnvävnad från patienter före och efter att de behandlats med DCA. Det de såg var uppmuntrande: en minskning av antalet cancerceller i hjärnvävnaden efter behandlingen.
Detta tillskrevs en ökad destruktion av dödliga celler och en minskad tillväxt av maligna glioblastoma multiforme-celler. Forskarna drog slutsatsen att en kombination av DCA och andra behandlingar kan vara en effektiv strategi mot GBM.
Forskargruppen föreslår att dikloracetat, som är känt för att vara giftfritt, används antingen före eller efter behandlingar som strålbehandling eller kirurgi. Detta tillvägagångssätt skulle potentiellt kunna öka fördelarna med standardbehandlingar för GBM.