Der Professor für Neurochirurgie und Onkologie an der Johns Hopkins University, Dr. Gregory Riggins, und seine Forschungsgruppe haben normalerweise wenig bis gar keine Schwierigkeiten, das Wachstum von Krebs in Testmäusen für ihre Studien zu ermöglichen.
Während einer Zeitspanne von mehreren Monaten im Jahr 2009 gab es jedoch eine Gruppe von Mäusen, bei denen die Tumorentwicklung einfach nicht stattfand. Bei näherer Betrachtung entdeckten sie, dass dieses unerwartete Ergebnis darauf zurückzuführen war, dass diesen Nagetieren Fenbendazol als Antiparasitikum verabreicht worden war.
„Bei unserer Untersuchung verschiedener Medikamente in dieser Gruppe erwies sich Fenbendazol als das wirksamste. Das hat unsere Aufmerksamkeit erregt“. Sagte die Forscherin
Als sich die Nachricht über seine Fähigkeiten verbreitete, entdeckte man, dass Fenbendazol allein oder in Kombination mit anderen Verfahren verabreicht werden kann, um das Krebswachstum zu heilen oder zu hemmen.
Riggins und Gallia und ihr Forschungsteam starteten einen Plan, um nicht nur die Funktionsweise dieses Medikaments zu verstehen, sondern auch seinen Nutzen gegen Glioblastomzellen zu verbessern und es für Patientenversuche zu produzieren. Nach der Überzeugung dieser Forscher hilft Fenbendazol bei der Blockierung der Tumorentwicklung, indem es die Bildung von Tubulinsträngen – Proteinen, die für die Vermehrung von Krebszellen unerlässlich sind – hemmt.
Dies geschah vor über einem Jahrzehnt. Heute, im Laufe der Zeit, haben wir ein umfangreiches Wissen über den wirksamen Einsatz von Fenbendazol gewonnen, um die Wahrscheinlichkeit zu erhöhen, dass wir Krebs ausrotten können.
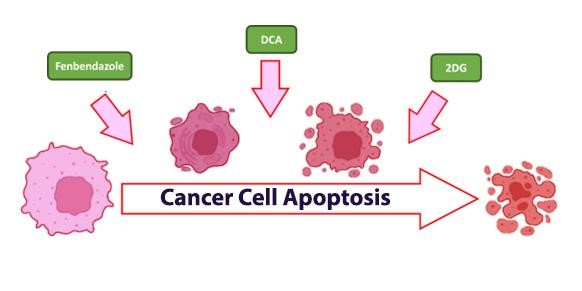
Die Energiestruktur des Krebses
Im Jahr 1923 machte Otto Heinrich Warburg – ein bedeutender deutscher Biochemiker, Mediziner und Nobelpreisträger – eine unschätzbare Entdeckung, die eine wichtige Rolle beim Verständnis des Energiestoffwechsels von Krebszellen spielte. Dieses beobachtete Phänomen gilt heute als das Schlüsselmerkmal von Krebs, das allgemein als „Warburg-Effekt“ bezeichnet wird.
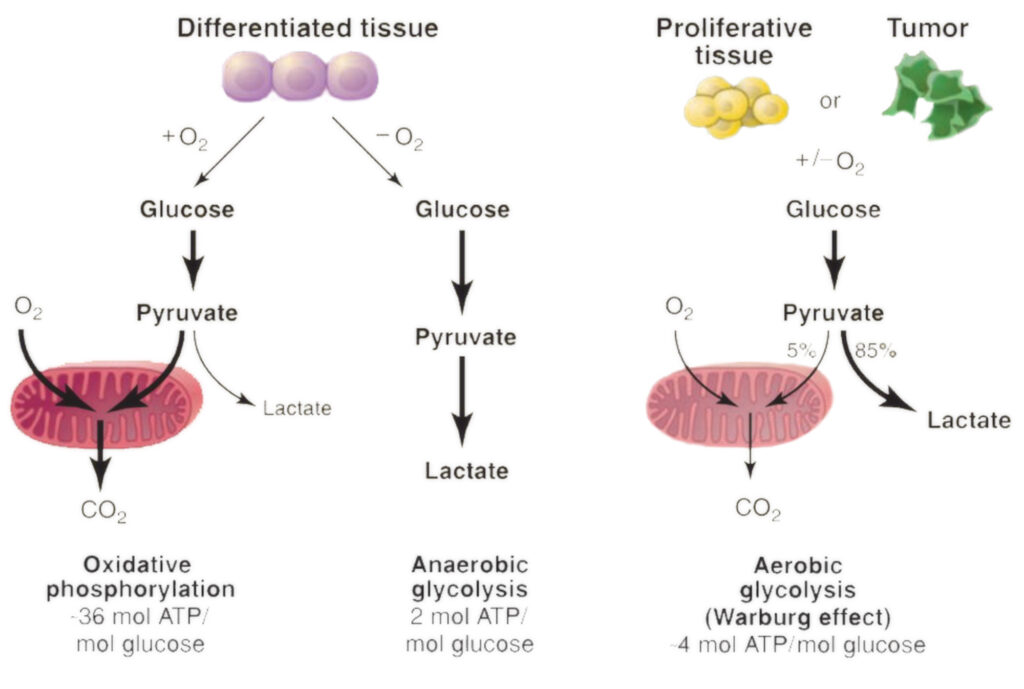
Eine bemerkenswerte Beobachtung machte Warburg bei der Untersuchung von Rattentumorzellen: Er stellte fest, dass diese auf außergewöhnlich hohen Glukosespiegeln (Zucker) gediehen und stattdessen den Sauerstoffverbrauch für Wachstumszwecke erhöhten, was kontraintuitiv erschien, da die Gewinnung von Energie aus Nährstoffen über höhere Nutzungsraten von Sauerstoff ein weitgehend effizienter Prozess gewesen wäre.
Die Etablierung solcher Erkenntnisse in jenen Zeiten vor etwa hundert Jahren weckte erhebliche Neugierde, die zu unbeantworteten Fragen führte, als dass Lösungen zur Hand gewesen wären.
Der enorme Glukosebedarf und der verringerte Sauerstoffverbrauch verschaffen den Krebszellen eine Reihe von evolutionären Vorteilen. Eine Art und Weise, in der der Warburg-Effekt bösartigen Zellen hilft, ist die Erleichterung einer schnellen Anhäufung von Biomasse. Die gesteigerte Aufnahme von Glukose versorgt das Tumorgewebe mit überschüssigen Bausteinen für die Bildung von neuem genetischen Material und Proteinen, was zu einer verstärkten Vermehrung und Ausbreitung von Krebs führt.
Außerdem ist es kein Geheimnis, dass normale Säugetierzellen einen konstanten Sauerstofffluss benötigen, da sie sonst schnell zugrunde gehen. Ihre erkrankten Gegenstücke verhalten sich jedoch völlig anders – das Wachstum von Tumoren übersteigt oft die verfügbare O2-Versorgung, verlangsamt sich aber aufgrund seiner adaptiven Natur nicht, sondern gedeiht unter solchen Umständen, ohne zu ersticken.
Nach kurzer Zeit stellen die Krebszellen ihren Stoffwechselprozess auf sauerstoffabhängige Glykolyse um. Sie beginnen, große Mengen an Milchsäure zu erzeugen und über die Zellgrenzen hinaus abzuführen, was zu einem Anstieg der sauren Bedingungen in der Tumorumgebung führt.
Der erhöhte Säuregehalt solcher Krebsumgebungen fördert das weitere Eindringen und die Ausbreitung, indem die zellverbindende extrazelluläre Matrix unseres Körpers abgebaut wird. Wenn dieser Säuregehalt ansteigt, hilft er den bösartigen Wucherungen, sich unserem Immunitätsmechanismus zu entziehen – einem inhärenten Schutz gegen Krankheiten wie diese. Dies ist zweifellos ein Grund dafür, dass die Immuntherapie in fortgeschrittenen Krebsstadien oft ihre Wirkung verliert.
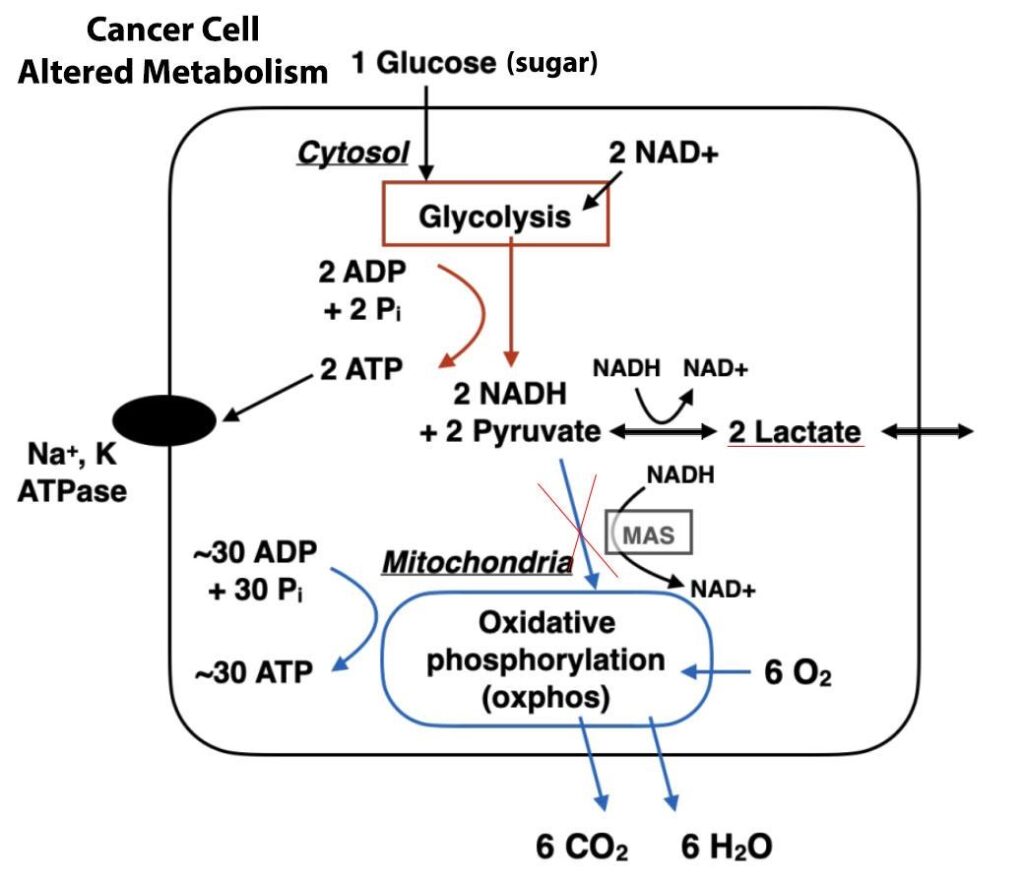
Gleichzeitig verbrauchen die Krebszellen weniger Sauerstoff, was dazu führt, dass die Mitochondrien in ihnen weniger reaktive Sauerstoffspezies erzeugen. Diese tragen entscheidend dazu bei, schädliche Krebszellen zu stoppen und zu vernichten. Die Krankheit beginnt, sich einem Mechanismus zu entziehen, der als Apoptose bezeichnet wird.
Die Apoptose ist ein gewöhnliches Phänomen, das in unserem Körper zum Tragen kommt; sie beseitigt unerwünschte oder überzählige Zellen, die ihre Existenz in der Anatomie fortsetzen.
Es handelt sich im Wesentlichen um einen natürlichen, vorbereiteten Zelltod, der das Tumorwachstum von Anfang an stoppt, indem er sich selbst vernichtet, um eine mögliche unnötige Ausbreitung dieser Tumore in uns zu verhindern, die Schäden verursachen, die nicht mehr repariert werden können, und so bösartige Zellkörper unschädlich zu machen.
Dies sind die wichtigsten metabolischen Vorteile, die ein unreguliertes Fortschreiten des Lebenszyklus verschiedener Transformationen ermöglichen, während sie aufgrund der Verhinderung des programmierten rechtzeitigen Todes (Apoptose) unbegrenzt unsterblich bleiben.
Besonders hervorzuheben ist dieser ziemlich verworrene Evolutionsprozess, den die neoplastischen Metamorphosen durchlaufen und der die Ärzte vor große Herausforderungen stellt, denn diese Krankheiten sind formidable Gegner, die komplexe Behandlungsprotokolle erfordern, aber wir sollten auch einen anderen Aspekt nicht vergessen, nämlich die Nutzung des Warburg-Effekts gegen krebserregende Substanzen.
Bei der Erkennung von Krankheiten hat sich die Menschheit dieses Phänomen des Krebsstoffwechsels zu Nutze gemacht. Der als Positronen-Emissions-Tomographie (PET) bekannte Test zeigt Gewebe und Organe mit ungewöhnlicher Stoffwechselaktivität an.
Da Krebszellen den Warburg-Effekt aufweisen, absorbieren sie radioaktive Glukose mit einer hundertmal höheren Rate als das sie umgebende normale Gewebe. Infolgedessen werden Tumore in den resultierenden Bildern beleuchtet, was eine einfache Verfolgung durch den gesamten Körper ermöglicht.
Was die Behandlung anbelangt, so könnte der Warburg-Paradigmenwechsel angesichts der Tatsache, dass sich fast alle bisherigen Krebsbehandlungen ausschließlich auf gentechnische Verfahren konzentrierten, als eine übersehene „Achillesferse“ in allen Ansätzen zur Behandlung von Krebserkrankungen über einen Zeitraum von fast einem Jahrhundert betrachtet werden. Eine alternative Verbindung – Natriumdichloracetat (DCA) – wirkt auf einzigartige Weise, indem sie abnormale Zellfunktionen im Zusammenhang mit dem Stoffwechsel wieder ins Gleichgewicht bringt
Notwendigkeit einer Immuntherapie
Krebszellen haben verschiedene Mechanismen entwickelt, um sich zu tarnen, so dass sie von der körpereigenen Immunabwehr nicht entdeckt werden können. Sie können genetische Mutationen aufweisen oder unterschiedliche Oberflächenproteine besitzen – beide Faktoren können das Immunsystem daran hindern, diese Zellen zu erkennen und zu bekämpfen.
In diesem Szenario spielen die TILs eine wichtige Rolle. Wenn die Tumore eines Patienten nicht aus diesen TILs bestehen, bedeutet dies, dass die Immunabwehr das Malignom nicht wirksam bekämpft, so dass eine immuntherapeutische Intervention erforderlich ist.
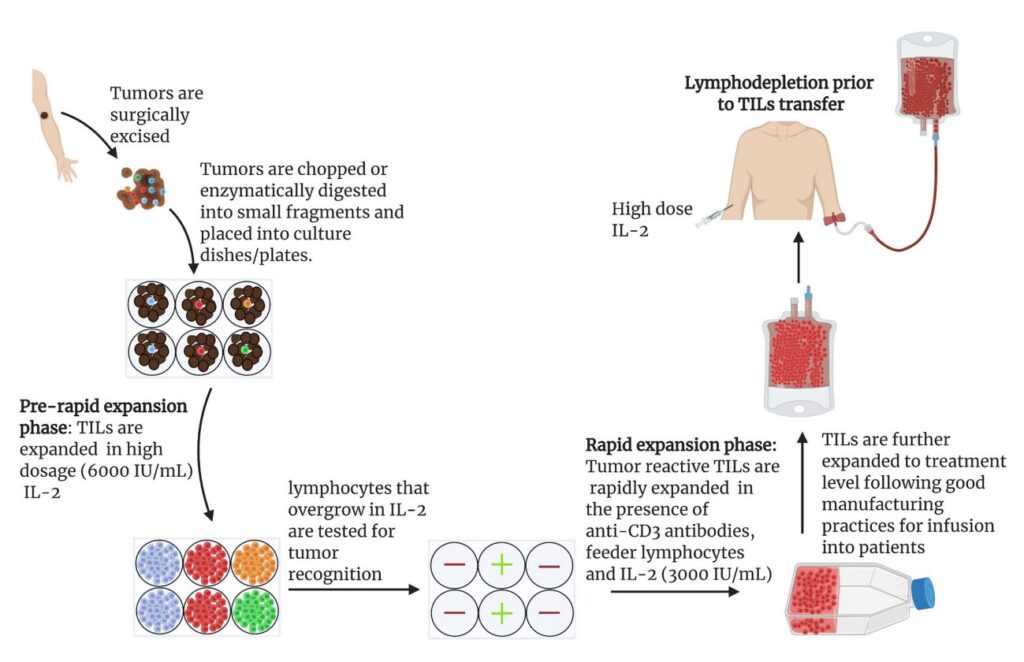
Schwierigkeiten bei der Krebsimmuntherapie
Die Krebsbehandlung ist mit der Immuntherapie in eine neue Phase eingetreten, die viele Menschen optimistisch stimmt. Dennoch ist dieser Ansatz nicht ohne Komplikationen. Ein Hauptproblem ist die Fähigkeit der Krebszellen, mit der Zeit eine Toleranz aufzubauen. Aufgrund ihrer hohen Energieproduktion über die Glykolyse blockieren diese schädlichen Zellen oft bestimmte Wege, die für die wirksame Steuerung der Funktionen der T-Zellen wichtig sind.
Wenn diese T-Zellen nicht richtig ausgereift sind, gelingt es ihnen nicht, die Tumorzellen erfolgreich zu identifizieren und zu neutralisieren, so dass sie stattdessen durch die Kraft der zuvor verabreichten therapeutischen Antikörper gefördert werden.
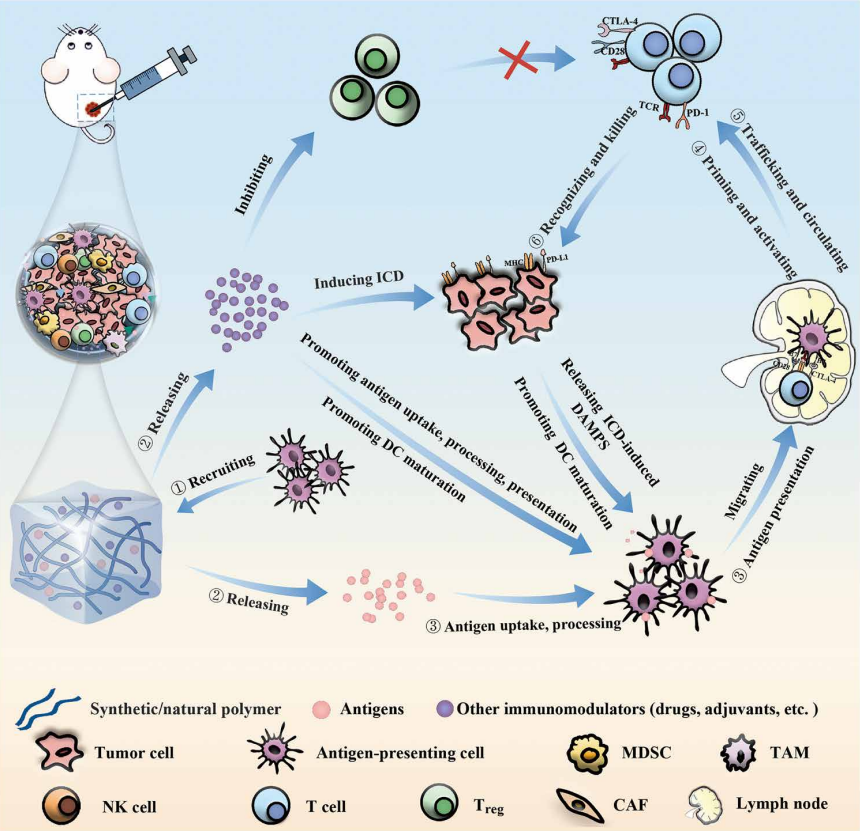
Die Schwierigkeiten angehen
Als Antwort auf diese Hürden könnte es sich als vorteilhaft erweisen, die Bemühungen auf die Hemmung des Energieproduktionssystems von Tumorzellen nach einer Immuntherapie zu richten. Indem man ihre Energieversorgung einschränkt, besteht die Möglichkeit, dass sie nicht mehr in der Lage sind, Signalwege zu blockieren, die die Entwicklung und Kontrolle der T-Zellen bestimmen.Neueste Erkenntnisse aus wissenschaftlichen Studien: 2-Desoxy-D-Glucose (2DG)
In der Krebsbehandlung, insbesondere bei dreifach negativem Brustkrebs (TNBC), gibt es eine spannende Entwicklung.
Wissenschaftler haben entdeckt, dass die Kombination einer Immuntherapie mit einem Glukose-Antimetabolit namens 2DG die Wirksamkeit der Behandlung verbessern könnte. Dies ist besonders bemerkenswert, weil TNBC-Zellen häufig hohe Konzentrationen eines Proteins namens PD-L1 (programmierter Todesligand 1) aufweisen.
Das Problem bei der Behandlung von TNBC ist, dass nur eine kleine Gruppe von Patienten, etwa 10 bis 20 %, tatsächlich positive Ergebnisse mit Therapien erzielt, die auf PD-L1 oder PD-1 abzielen, die Schlüsselakteure bei der Immunantwort des Körpers sind.
Dieser neue Ansatz, bei dem 2DG zum Einsatz kommt, könnte für viele TNBC-Patientinnen, die derzeit nur begrenzt auf eine Behandlung ansprechen, eine Wende bedeuten.
Ein wichtiger Punkt: Eine bestimmte Form von PD-L1, das so genannte glykosylierte PD-L1, ist für die Wechselwirkungen zwischen PD-L1 und PD-1 entscheidend. Darüber hinaus weisen Zellen, die mit TNBC assoziiert sind, im Vergleich zu Nicht-TNBC-Zellen tendenziell höhere Werte dieses glykosylierten PD-L1 auf.
Die Forschung hat gezeigt, dass die Glykosylierung von PD-L1 reduziert werden kann, indem die Stabilität und Funktion dieses immunhemmenden Pro-Krebs-Moleküls erheblich beeinflusst wird.
Hier kommt die „Desoxyglukose“ ins Spiel. Die Verwendung von Desoxyglukose kann diesen Prozess möglicherweise unterbrechen und zu neuen Strategien führen, die verschiedene Ansätze für wirksamere TNBC-Behandlungsergebnisse kombinieren.
Techniken der Krebsbehandlung: Konventionelle und fortschrittliche Methoden
Auf dem Weg zu wirksamen Lösungen für Krebserkrankungen gibt es zahlreiche Methoden, die von konventionellen bis hin zu avantgardistischen Techniken reichen.
Etablierte Behandlungsverfahren wie Chemo- und Strahlentherapie sind weithin anerkannt, während neuartige Elemente wie 2DG aufgrund ihrer voraussichtlichen Vorteile bei der Behandlung von Krebs zunehmend an Attraktivität gewinnen, sei es einzeln oder in Ergänzung zu bewährten Hilfsmitteln wie Fenbendazol und DCA, die ebenfalls erheblich zur Bekämpfung der Krankheit beitragen.

Chemotherapie
Der Einsatz von Chemotherapie ist nach wie vor ein zentrales Element bei der Bekämpfung der Krankheit Krebs. Sie ist besonders wirksam bei Erkrankungen wie Brustkrebs, wo sie eingesetzt wird, um den Tumor zu verkleinern und die chirurgische Entfernung zu erleichtern – ein Ansatz, der als präoperative Chemotherapie oder PCT bezeichnet wird.
Doch auch wenn sie den Tumor verkleinern kann, können wir uns nicht immer auf diese Methode allein verlassen, denn es gibt zahlreiche Fälle, in denen die bösartigen Zellen nach der Behandlung wieder auftauchen.
Verstärkung der Wirkung der Chemotherapie durch 2DG
Studien deuten darauf hin, dass die Verknüpfung von Chemotherapie und 2DG ihre Wirksamkeit verstärken könnte. 2DG ähnelt in seiner Funktion der Glukose und ist in der Lage, in die Stoffwechselaktivitäten der Krebszellen einzugreifen, was die Wirkung der regulären Chemotherapie verstärken könnte.
Die doppelte Verwendung symbolisiert das Potenzial für eine umfassende pathologische Reaktion, was bedeutet, dass stärkere und länger anhaltende Behandlungsergebnisse erzielt werden können. Zahlreiche Labortests und Tierstudien wurden durchgeführt, um diese kombinierte Strategie zu bestätigen.
Strahlentherapie
In Krebszellen ist 2DG die alleinige Methode zur Regulierung des Zuckerstoffwechsels, aber es wird auch mit Therapieformen wie Chemotherapie und Strahlentherapie kombiniert.
Realistisch betrachtet, spielt die Strahlentherapie eine entscheidende Rolle bei der Behandlung von Krebs. Etwa 60 % der Menschen, die mit dieser grausamen Krankheit zu kämpfen haben, werden mit dieser Art von Behandlung behandelt, entweder allein oder in Verbindung mit anderen Behandlungen.
Die Strahlentherapie ist zwar ein wirksames Mittel im Kampf gegen den Krebs, aber sie ist auch nicht unproblematisch. Sie ist zweifelsohne wirksam, kann aber mit der Zeit einige unerwünschte Nebenwirkungen haben. Eine große Sorge ist, dass Krebszellen eine Resistenz gegen die Strahlung entwickeln könnten, und es besteht auch die Gefahr, dass gesunde Zellen geschädigt werden.
Um diese Probleme anzugehen, insbesondere das Problem der Strahlungstoleranz, ist es wichtig, Glykolysehemmer in die Behandlung einzubeziehen. Diese Inhibitoren unterbrechen die Energiezufuhr zu den Krebszellen und entziehen ihnen so die benötigten Nährstoffe.
Dadurch wird es den Krebszellen erschwert, sich nach einer Bestrahlung selbst zu reparieren, was schließlich zu ihrem Zusammenbruch und ihrer Zerstörung führt. Ein solcher Ansatz ist ein Schritt nach vorn, um die Strahlentherapie für die Patienten sicherer und wirksamer zu machen.
Verstärkung der Strahlentherapie durch 2-Deoxy-D-Glucose
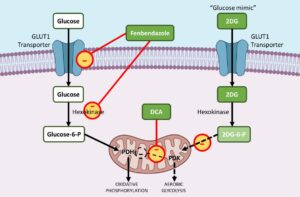
2DG dient als Glykolytik-Inhibitor. Seine Funktion besteht in der Bindung an das Glukosetransportprotein GLUT1, bevor es durch das Enzym Hexokinase phosphoryliert wird. Seine metabolische Entwicklung endet jedoch dort, so dass der glykolytische Weg blockiert bleibt.
Krebszellen, die diesem Inhibitor ausgesetzt sind, können aufgrund der Unterbrechung des normalen Glukose-Glykolyseprozesses keine Energie mehr produzieren. Außerdem regt 2DG die Funktionen der Enzyme Caspase 3 und PARP an, die in den bösartigen Zellen zur Apoptose führen, während gesunde Zellen davon unberührt bleiben.
In der Krebsbehandlung zeichnet sich eine vielversprechende Kombination ab: 2-Desoxy-D-Glucose (2DG) in Kombination mit Strahlentherapie. Dieses Duo könnte die Wirkung der Strahlentherapie erheblich verstärken. Wie das?
Nun, 2DG wirkt als Glukoseinhibitor. Es stört die Fähigkeit der Krebszellen, sich nach einer Strahlenschädigung selbst zu reparieren, vor allem weil diese Zellen nicht genügend Glukose und wichtige Nährstoffe erhalten.
Aber 2DG ist nicht nur ein One-Trick-Pony. Es erfüllt mehrere Zwecke. Es ist nicht nur ein Disruptor, sondern verstärkt auch die Wirkung einer Strahlenbehandlung. Seine Wirkung hängt mit der Veränderung des Gleichgewichts der Oxidations-Reduktionsprozesse in den Zellen zusammen.
Ein wichtiger Aspekt dabei ist, dass der oxidative Stress vermutlich ein Schlüsselweg ist, über den ionisierende Strahlung Krebszellen abtötet. Dieser neue Ansatz, bei dem 2DG in Verbindung mit einer Strahlentherapie eingesetzt wird, könnte einen Wendepunkt in der wirksamen Behandlung von Krebs darstellen.
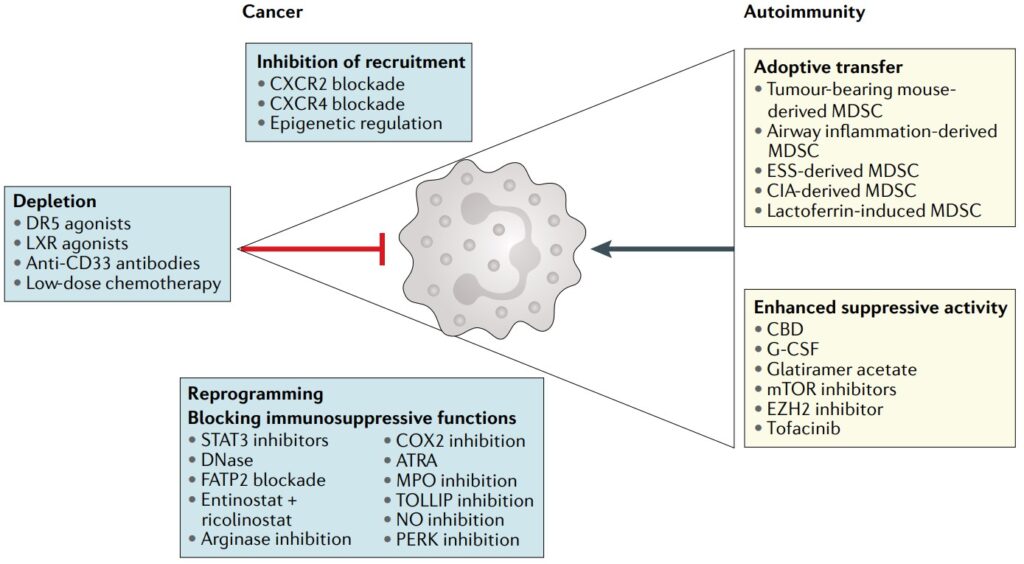
Krebszellenvielfalt
Krebszellen sind ein vielfältiger Haufen, den die Wissenschaftler als Tumorheterogenität bezeichnen und den man bei fast jeder Krebsart findet. Diese Vielfalt ist oft auf Fehler zurückzuführen, die bei der DNA-Replikation während der Zellteilung gemacht werden.
Das geschieht folgendermaßen: Wenn bei der Teilung von Zellen Fehler beim Kopieren ihrer DNA auftreten, entstehen neue Zellen mit Mutationen. Mit der Zeit, insbesondere wenn bestimmte Umweltfaktoren als Auslöser wirken, können sich diese mutierten Zellen weiterentwickeln und möglicherweise zu Krebs führen. Es ist ein langsamer Prozess, aber so beginnen viele Krebsarten ihre Reise.
Verschiedene Formen der Ungleichheit bei Krebs
Die bei Krebszellen beobachtete Differenzierung, die als Tumorheterogenität bezeichnet wird, lässt sich vereinfacht in zwei Bereiche einteilen:
Räumliche Tumorheterogenität
Das bedeutet, dass sich die Krebszellen nicht gleichmäßig über das betroffene Gewebe verteilen. Stattdessen neigen sie dazu, sich auf zufällige und unvorhersehbare Weise auszubreiten.
Zeitliche Schwankungen der Tumorvielfalt
Wenn sich Tumoren im Laufe der Zeit entwickeln, bilden sie oft verschiedene Subtypen aus. Dieser Prozess wird als zeitliche Heterogenität bezeichnet. Grundsätzlich gilt: Je länger ein Tumor wächst, desto vielfältiger kann er werden.
Die unterschiedlichen Eigenschaften von Tumorzellen stellen ein großes Hindernis bei der wirksamen Bekämpfung von Krebs dar. Die Vielfalt dieser bösartigen Zellen führt häufig zu einer Resistenz gegenüber den derzeitigen therapeutischen Strategien.
Angesichts dieser Komplexität des Krebsverhaltens besteht ein dringender Bedarf an der Entwicklung von Behandlungen, die wirksam auf die Resistenz abzielen und diese überwinden können, die durch die unterschiedliche genetische Beschaffenheit der einzelnen Krebszellen verursacht wird.
Ergebnisse der Studie
Eine Vielzahl von Studien, darunter Labortests, Tierversuche und klinische Studien am Menschen, haben sich eingehend mit den Auswirkungen von 2-Desoxy-D-Glucose (2DG) auf Zellen befasst. Aus dieser Forschung geht hervor, dass 2DG auf komplexe Weise wirkt.
Es stoppt nicht nur den Prozess der zellulären Glykolyse, sondern fördert auch die Apoptose, den programmierten Zelltod, ohne gesunde Zellen zu schädigen. Darüber hinaus beeinflusst 2DG das Verhalten von Genen in den Zellen.
Es unterbricht Transkriptionsfaktoren, die für die Aktivierung von Genen, die für die Zellreplikation wichtig sind, entscheidend sind. Diese Erkenntnis deutet auf das Potenzial von 2DG als Waffe gegen verschiedene Eigenschaften von Krebszellen hin.
Eine Besonderheit von Krebszellen sind ihre vielfältigen genetischen Mutationen, die für das Fortschreiten der Krankheit eine Rolle spielen. Eines haben sie jedoch alle gemeinsam: eine höhere Rate des Zuckerstoffwechsels im Vergleich zu normalen Zellen.
Dies macht 2DG zu einer potenziell wirksamen Behandlung für eine Vielzahl von Krebsarten. Es wirkt, indem es den Krebszellen Zucker und Sauerstoff entzieht und gleichzeitig ihre Genaktivität beeinträchtigt. Auf diese Weise kann das Zellwachstum verlangsamt und die Zellen in Richtung Selbstzerstörung gelenkt werden, was ein übermäßiges Wachstum verhindert.
Aussichtsreiche Heilung für Glioblastom-Krebs
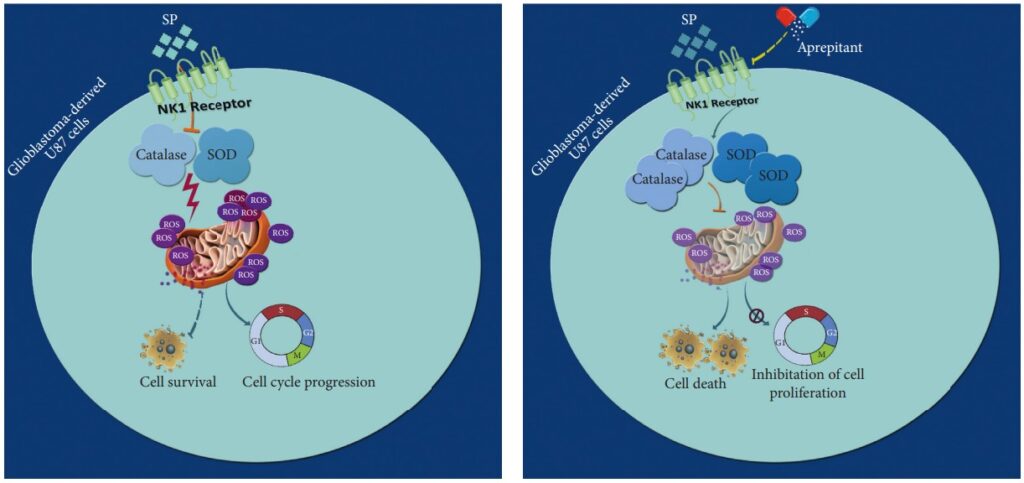
Das Glioblastom ist eine besonders aggressive Form von Hirntumor, die sich durch eine starke Resistenz gegenüber dem Zelltod und den begrenzten Erfolg der derzeitigen Behandlungen auszeichnet. Diese Situation unterstreicht die dringende Notwendigkeit, neue Behandlungsmöglichkeiten zu erforschen.
Vor nicht allzu langer Zeit begannen Dr. Evangelos Michelakis, ein engagierter medizinischer Wissenschaftler, und sein Team mit mehreren Forschungsprojekten, die sich auf die Therapie des Glioblastoma multiforme (GBM) konzentrierten. Sie erkannten, dass eine ideale Behandlung in der Lage sein sollte, die Blut-Hirn-Schranke zu überwinden und Krebszellen gezielt anzugreifen, ohne gesundes Gewebe zu schädigen.
Die von ihnen gewählte Substanz, Natriumdichloracetat (DCA), wies diese Eigenschaften auf und, was besonders wichtig war, zeigte keine Anzeichen für eine Schädigung von Blut, Herz, Nieren oder Leber.
Diese Entdeckung veranlasste sie zur Durchführung einer bahnbrechenden Studie mit echten Patienten, die den Weg für weitere bahnbrechende Erkenntnisse bei der Behandlung von GBM ebnete.
Der Einfluss von DCA auf das Absterben von Krebszellen und die Tumorentwicklung
Es wird immer deutlicher, dass Dichloracetat (DCA) einen bedeutenden Einfluss auf die Krebsbekämpfung hat, insbesondere im Fall des Glioblastoms, einer tödlichen Form von Hirnkrebs. DCA ist in der Lage, den Tod von Krebszellen auszulösen, die Blutgefäße, die den Tumor versorgen, zu verkleinern und das Wachstum dieses aggressiven Krebses zu verlangsamen.
Besonders vielversprechend ist, dass DCA am wirksamsten sein könnte, wenn es zusammen mit anderen Behandlungen eingesetzt wird, was einen neuen Hoffnungsschimmer im Kampf gegen diese schwierige Krankheit darstellt.
Neben anderen Therapien für Glioblastome
Bei einer seltenen Gelegenheit hatten die Wissenschaftler die Möglichkeit, Gehirngewebe von Patienten vor und nach der Behandlung mit DCA zu vergleichen. Was sie sahen, war ermutigend: ein Rückgang der Krebszellen im Hirngewebe nach der Behandlung.
Dies wurde auf eine verstärkte Zerstörung tödlicher Zellen und eine Verringerung des Wachstums bösartiger Zellen des Glioblastoma multiforme zurückgeführt. Die Forschung kam zu dem Schluss, dass die Kombination von DCA mit anderen Behandlungen eine wirksame Strategie gegen GBM sein könnte.
Das Forschungsteam schlägt vor, Dichloracetat, das als ungiftig bekannt ist, entweder vor oder nach Verfahren wie Strahlentherapie oder Operation einzusetzen. Dieser Ansatz könnte die Vorteile der Standardbehandlungen für GBM potenziell verstärken.